

| A. | 电池工作时,负极附近溶液的pH升高 | |
| B. | 电路中转移2mol电子,理论上约消耗标准状况下空气56L | |
| C. | 电池工作时,电流由M极经外电路流向N极 | |
| D. | 电池总反应为4Al+3O2=2Al2O3、2Mg+O2=2MgO |
分析 根据原电池的工作原理可以看出:活泼金属镁和铝的合金是负极,该电极上发生失电子的氧化反应,正极上是氧气得电子的还原反应,电子从负极流向着正极,电流从正极流向负极,总反应是正极和负极反应的和,根据电极反应式来回答.
解答 解:A、根据原电池的工作原理可以看出:活泼金属镁和铝的合金是负极,该电极上发生失电子的氧化反应,即Mg-2e-=Mg2+,正极上是氧气得电子的还原反应,产生氢氧根离子,氢氧根离子和镁离子之间反应会得到氢氧化镁,负极附近溶液的pH降低,故A错误;
B、电路中转移2mol电子,根据正极上发生反应:O2+4H++4e-=2H2O,消耗氧气的物质的量是0.5mol,标况下的体积是11.2L,理论上约消耗标准状况下空气56L,故B正确;
C、电池工作时,电流从正极流向负极,即由N极经外电路流向M极,故C错误;
D、电池总反应为2Mg+O2+2H2O=2Mg(OH)2↓,故D错误.
故选B.
点评 本题综合考查原电池知识,为高频考点,侧重于学生的分析能力的考查,侧重于正负极的判断和电极方程式的书写,学生要注意相关基础知识的积累,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1mol酸与1mol碱完全反应放出的热量就是中和热 | |
| B. | 如果反应在加热时才能发生,则该反应是吸热反应 | |
| C. | 反应物总能量大于生成物总能量,则反应的△H<0 | |
| D. | 强酸强碱中和热的离子方程式可表示为:H+(aq)+OH-(aq)═H2O(l)△H=57.3 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
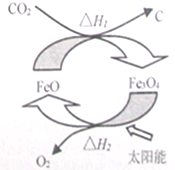
| A. | 由二氧化碳制取碳和氧气的反应为放热反应 | |
| B. | 该循环反应中,FeO的质量减小 | |
| C. | 根据盖斯定律可知,△H1+△H2=0 | |
| D. | 该反应是将太阳能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应化学方程式为CO+H2O?CO2+H2 | |
| B. | 该反应为吸热反应 | |
| C. | 升高温度,逆反应速率减小 | |
| D. | 无论采取怎样的措施该体系中混合气体的平均分子量都不会发生改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸、水 | B. | 饱和食盐水、浓H2SO4 | ||
| C. | 烧碱、石灰水 | D. | 无水CaCl2、烧碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸乙酯和水,乙醇和水,己烯和水 | |
| B. | 二溴乙烷和水,溴苯和水,硝基苯和水 | |
| C. | 己烷和水,乙醛和水,乙酸和乙醇 | |
| D. | 乙酸和水,甲苯和水,己烷和己烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe分别与氯气和稀盐酸反应所得氯化物不同 | |
| B. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 | |
| C. | SO2、NO2都能与水反应,其反应原理相同 | |
| D. | N2的化学性质通常非常稳定,但在放电条件下可以与O2反应生成NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+ H+ NO3- Fe2+ | B. | Ca2+ NO3- HCO3- OH- | ||
| C. | K+ H+ Cl- SO42- | D. | Fe3+ Cl- H+ CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com