
a mol FeS与b mol FeO投入到V L、c mol/L的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )
①(a+b)×63 g ②(a+b)×189 g ③(a+b)mol ④[Vc-(9a+b)/3]mol
A.①④ B.②③ C.①③ D.②④
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练7-1练习卷(解析版) 题型:填空题
溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)
=0.100 mol/L、c(B)=0.200 mol/L及c(C)=0 mol/L。反应物A的浓度随时间的变化如图所示。
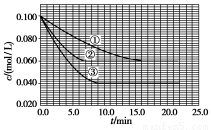
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
② ;
③ 。
(2)实验②平衡时B的转化率为 ;实验③平衡时C的浓度为 。
(3)该反应的ΔH 0,其判断理由是 。
(4)该反应进行到4.0 min时的平均反应速率:
实验②:v(B)= 。
实验③:v(C)= 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练5-2练习卷(解析版) 题型:填空题
位于短周期的四种元素A、B、C、D,其原子序数依次增大。A在周期表中原子半径
最小;B是地壳中含量最高的元素;B、D位于同一主族;C的原子半径在同周期中最大。回答下列问题:
(1)写出由上述元素形成的具有漂白作用的3种物质的化学式: 、 、 。
(2)写出含B元素质量分数最高的化合物的电子式: 。
(3)分别由A、B、C、D四种元素组成的两种化合物X和Y可以发生反应,试写出该反应的离子方程式: 。
(4)用电子式表示化合物C2B的形成过程: 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练5-1练习卷(解析版) 题型:选择题
科学家从化肥厂生产的(NH4)2SO4中检验出组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO42-和N2H44+两种离子形式存在,植物的根系极易吸收N4H44+,但它遇到碱时,会生成一种形似白磷的N4分子。N4分子不能被植物吸收。下列有关说法不正确的是( )
A.N4和N2互为同素异形体
B.14N与14C互为同位素
C.N4H4(SO4)2不能与草木灰混合使用
D.8NH3+4C5OH=N4+4C5NH2+6H2+4H2O,此反应中每生成5.6 g N4时转移1.2 mol电子
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练5-1练习卷(解析版) 题型:选择题
锎是锕系中的一种元素,1 mg锎(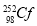 )每秒钟约能释放出2.34×109个中子,在医学上常用作治疗恶性肿瘤的中子源。下列有关说法错误的是( )
)每秒钟约能释放出2.34×109个中子,在医学上常用作治疗恶性肿瘤的中子源。下列有关说法错误的是( )
A.锎位于元素周期表第6周期
B.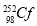 和
和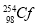 互为同位素
互为同位素
C.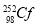 中,质子数和电子数均为98
中,质子数和电子数均为98
D.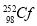 的中子数与质子数之差为56
的中子数与质子数之差为56
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练4-4练习卷(解析版) 题型:选择题
已知常温常压下在1 L水中可溶解40 L NO2,NO2能与NaOH溶液发生反应:2NaOH+2NO2=NaNO3+NaNO2+H2O。以下各种尾气吸收装置中,不适合吸收NO2气体的是( )

查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练4-3练习卷(解析版) 题型:填空题
现有四个无标签的试剂瓶,分别盛有硫酸、BaCl2溶液、盐酸和不知名称的某正盐溶液M,将四种试剂分别标为A、B、C、D,取少量试剂分别进行实验得到如表格所示关系(其中无色气体能使澄清石灰水变浑浊,M溶液进行焰色反应为黄色)。
ABCD
A白色沉淀X白色沉淀Y
B白色沉淀X无色气体
(1)写出试剂名称:A ,B 。
(2)写出生成X的离子方程式: 。
(3)有人认为M是Na2CO3,此结论是否正确 (填“正确”或“不正确”),如认为正确,请说明推断的依据 ,如不正确,请说明理由 。
(4)若A、硝酸、D三种溶液混合后仍有沉淀,则其反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练4-2练习卷(解析版) 题型:选择题
氯气是一种重要的工业原料。工业上利用反应3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是( )
A.若管道漏气遇氨就会产生白烟
B.该反应利用了Cl2的强氧化性
C.该反应属于复分解反应
D.生成1 mol N2有6 mol电子转移
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练3-3练习卷(解析版) 题型:选择题
将11.9 g由Mg、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7 g。
另取等质量的合金溶于过量稀硝酸中,生成了6.72 L NO(标准状况下),向反应后的溶液中加入适量NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,则沉淀的质量为( )
A.22.1 g B.27.2 g
C.30 g D.无法计算
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com