
向100mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如下图所示。则下列说法中正确的是( )
A.c点溶液呈碱性
B.b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH— =
Al(OH)3↓+2BaSO4↓
C.c点加入Ba(OH)2溶液的体积为200 mL
D.a点的溶液呈中性

科目:高中化学 来源: 题型:
合成氨工业中,原料气(N2、H2、混有少量CO、NH3)在进入合成塔之前,常用醋酸二氨合铜(Ⅰ)溶液来吸收CO,其反应为CH3COO[Cu(NH3)2]+CO+NH3
CH3COO[Cu(NH3)3]·CO(正反应为放热反应)。
(1)必须除去CO的原因是_______________________________________。
(2)醋酸二氨合铜(Ⅰ)溶液吸收原料气中CO的适宜条件是
____________________________________________________。
(3)吸收CO后的醋酸铜(Ⅰ)氨溶液经适当处理又可再生,恢复其吸收CO的能力而循环使用,其再生的条件是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向一定量的Fe、FeO、Fe2O3的混合物中,加入100mL 1mol/L的盐酸,恰好使混合物完全溶解,放出224mL(标况)的气体,经测定所得溶液中无Fe3+,若用足量的CO在高温下还原相同质量的此混合物,能得到的铁的质量为( )
A.11.2g B.5.6g C.2.8g D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
室温时,盐酸和硫酸的混合溶液20mL,向混合物中逐滴加入0.05mol·L-1Ba(OH)2溶液时,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化)。下列说法正确的是
A.图中A点对应溶液的pH:a=1
B.生成沉淀的最大质量m=2.33g
C.原混合液中c(HCl)=0.2mol·L-1
D.当V[Ba(OH)2(aq)]=30mL时,有关离子浓度大小:
c(Cl-)>c(Ba2+)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:
①2NO(g)+O2(g) 2NO2(g)
2NO2(g)
②2NO2(g) N2O4(g)
N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃, 10min后升高并维持容器的温度为T2℃。下列说法正确的是( )
A.前5min反应的平均速率v(N2O4)=0.18mol·L-1·s-1
B.T1℃时反应②的化学平衡常数K=0.6
C.反应①、②均为吸热反应
D.若起始时向该容器中充入3.6mol NO2和2. 0mol N2O4,T1℃达到平衡时,N2O4的转化率为10%
查看答案和解析>>
科目:高中化学 来源: 题型:
反应:L(s)+aG(g)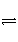
 bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中
bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中
压强p1>p2,x轴表示温度,y轴表示平衡时混合气体中G的体积分数。据此可判断( )

①上述反应是放热反应 ②上述反应是吸热反应 ③a>b ④a<b
A.①③ B.①④ C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,向一个容积不变的容器中,通入2 mol A2和8 mol B2及固体催化剂,使之反应。已知:A2(g)+3B2(g)
 2AB3(g) ΔH=-Q kJ·mol-1。平衡时容器内气体压强为起始时的80%。
2AB3(g) ΔH=-Q kJ·mol-1。平衡时容器内气体压强为起始时的80%。
(1)平衡时容器内AB3的体积分数为________。
(2)加入2 mol A2和8 mol B2,达平衡时,放出热量为________(填序号)。
A.小于Q kJ B.等于Q kJ
C.大于Q kJ D.可能大于或小于或等于Q kJ
(3)在相同的容器中,降低温度,通入2 mol AB3和1 mol B2及固体催化剂,反应达平衡时对AB3的体积分数,下列判断正确的是________(填序号)。
A.一定等于1/4 B.一定大于1/4
C.一定小于1/4 D.可能大于或小于或等于1/4
理由是_________________________________________________________________。
(4)保持同一温度,在相同容器中,起始通入一定物质的量的A2、B2、AB3,欲使平衡时AB3的体积分数为1/4,且起始时反应表现为向正反应方向进行,则充入A2的物质的量a mol的取值范围是_______________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com