
分析 (1)根据元素X的气态氢化物的化学式确定元素X的最低负价,而元素的最高正价+|最低负价|=8,进而求得X元素最高正价,结合选项各化学式中X元素的化合价;
(2)氧元素的近似相对原子量为各原子的相对原子量与其百分含量之积的和;
(3)H2O和D2O物质的量相等时,与足量钠反应生成的H2、D2物质的量相等,然后根据m=nM计算生成气体质量之比;
(4)X2-含中子N个,X原子含有质子数=质量数-中子数=A-N,X的氢化物为H2X,该氢化物中含有质子数=A-N+2,然后结合n=$\frac{m}{M}$计算;
(5)钾和另一种碱金属在化合物中的化合价均为+1价,计算出氢气的物质的量,然后根据2M+2H2O═2MOH+H2↑计算金属的物质的量及摩尔质量,利用平均摩尔质量的来解答.
解答 解:(1)元素X的气态氢化物的化学式为XH4,所以X的最低负价为-4价,所以元素R的最高正价为+4价,X的最高价氧化物的水化物的化学式为H2XO3,
故答案为:H2XO3;
(2)16O、17O、18O在自然界中所占的原子个数百分比分别为:a%、b%、c%,则氧元素的近似相对原子质量为:16a%+17b%+18c%,
故答案为:16a%+17b%+18c%;
(3)物质的量相同的H2O和D2O与足量钠反应生成的H2、D2物质的量相等,放出的气体的质量之比语气摩尔质量成正比,则生成气体的质量之比=2g/mol:4g/mol=1:2,
故答案为:1:2;
(4)X2-含中子N个,X原子X2-含有中子数相同,则X原子的质子数=A-N,X的氢化物为H2X,该氢化物中含有质子数=A-N+2,1gH2X的物质的量为:$\frac{1g}{(A+2)g/mol}$=$\frac{1}{A+2}$mol,1g X的氢化物中含质子的物质的量是:$\frac{1}{A+2}$mol×A-N+2=$\frac{A-N+2}{A+2}$mol,
故答案为:$\frac{A-N+2}{A+2}$;
(5)氢气的物质的量为:$\frac{0.2g}{2g/mol}$=0.1mol,
由2M+2H2O═2MOH+H2↑,
2 1
0.2mol 0.1mol
则金属的平均摩尔质量为:$\frac{4.2g}{0.2mol}$=21g/mol,
铷的摩尔质量为85.5g/mol,则另一种碱金属的摩尔质量一定小于21g/mol,碱金属元素中摩尔质量小于21g/mol的只有Li,则另一碱金属可能是Li,
故答案为:Li.
点评 本题考查较为综合,涉及化学方程式的计算、物质的量的计算、原子结构与元素周期律的应用等知识,题目难度中等,明确原子构成、物质的量与其它物理量之间的关系为解答关键,试题知识点较多,充分考查了学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在离子化合物中不可能含有共价键 | |
| B. | 在共价化合物中也可能含有离子键 | |
| C. | 凡含有离子键的化合物一定是离子化合物 | |
| D. | 完全由非金属元素组成的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
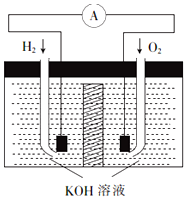 氢氧燃料电池是符合绿色化学理念的新型发电装置.其工作原理如图所示,该电池的电极表面镀了一层细小的铂粉,已知铂吸附气体的能力强,且性质稳定.
氢氧燃料电池是符合绿色化学理念的新型发电装置.其工作原理如图所示,该电池的电极表面镀了一层细小的铂粉,已知铂吸附气体的能力强,且性质稳定.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属与非金属元素形成的化合物一定是离子化合物 | |
| B. | 干冰气化过程中只需克服分子间作用力 | |
| C. | HF的热稳定性很好,是因为HF分子间存在氢键 | |
| D. | 常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 项目 | 分析 |
| A | 制备乙烯、制备硝基苯 | 实验时均用到了温度计 |
| B | 乙烯制备乙醇、氯乙烷制备乙醇 | 属于同一反应类型 |
| C | 丙烯可以使溴水和酸性高锰酸钾溶液褪色 | 褪色原理不同 |
| D | 乙醇燃烧、乙醇使重铬酸钾变色 | 均为氧化反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水浴加热 | B. | 将稀硫酸改为98%的浓硫酸 | ||
| C. | 滴加少许CuSO4溶液 | D. | 改用铁粉并振荡 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com