
【题目】硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如图,下列说法正确的是( )
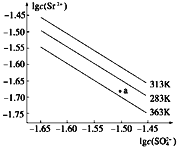
A. 283 K时,图中a点对应的溶液是不饱和溶液
B. 三个不同温度下,363 K时Ksp(SrSO4)最大
C. 温度一定时,Ksp(SrSO4)随c(SO42-)的增大而减小
D. 283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的四种短周期元素。n、p、r是由这些元素组成的二元化合物。m 是元素W的单质。q是元素Y的单质且是制作太阳能电池的原料。p在常温下为常见无色液体,0.010mol·L-1的r溶液中c(H+)为0.010 mol·L-1,s是弱酸且不溶于水。上述物质的转化关系如图所示。下列说法不正确的是
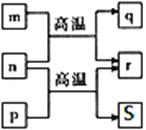
A.r易溶于p
B.原子半径:Z<Y
C.最高价氧化物对应水化物的酸性:Y<Z
D.最简单氢化物的稳定性:X<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业中很多重要的化工原料都来源于石油化工,如图中的苯、丙烯、有机物A等,其中A的产量可以用来衡量一个国家的石油化工发展水平。请回答下列问题:
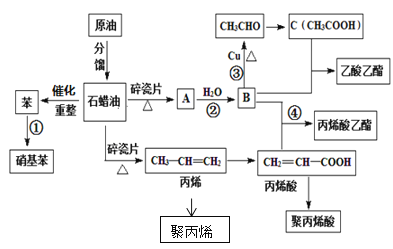
(1)A的结构简式为__,丙烯酸中官能团的名称为___。
(2)写出下列反应的反应类型①__,③___。
(3)用一种方法鉴别B和C,所用试剂是__。
(4)写出下列反应方程式:
丙烯→聚丙烯__;
丙烯酸+B→丙烯酸乙酯__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,电解质溶液的性质与变化是多样的,下列说法正确的是( )
A. pH相同的①CH3COONa ②NaClO ③NaOH三种溶液c(Na+)大小:①>②>③
B. 往稀氨水中加水,![]() 的值变小
的值变小
C. pH=4的H2S溶液与pH=10的NaOH溶液等体积混合,存在下列等式:c(Na+)+c(H+)c=(OH—)+2c(S2—)
D. Ca(ClO)2溶液中通入少量CO2,ClO—水解程度增大,溶液碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. Fe与S混合加热生成FeS2
B. NaHCO3的热稳定性大于Na2CO3
C. 过量的铜与浓硝酸反应有一氧化氮生成
D. 白磷在空气中加热到一定温度能转化为红磷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2作为一种广谱型的消毒剂,将逐渐用来取代Cl2成为自来水的消毒剂。已知ClO2是一种易溶于水而难溶于有机溶剂的气体,11℃时液化成红棕色液体。
(1)某研究小组用如图装置制备少量ClO2(夹持装置已略去)。
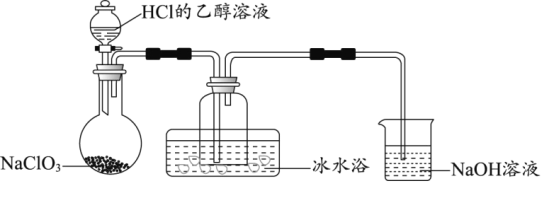
①冰水浴的作用是___。
②NaOH溶液的主要作用为吸收反应产生的Cl2,其吸收液可用于制取漂白液,该吸收反应的离子方程式为___,该反应的氧化剂与还原剂物质的量之比为___。
③以NaClO3和HCl为原料制备ClO2,完成化学方程式___。
(2)将ClO2水溶液滴加到KI溶液中,溶液变棕黄;再向其中加入适量淀粉溶液,振荡、静置,观察到___,证明ClO2具有氧化性。
(3)ClO2在杀菌消毒过程中会产生Cl-,用0.0001mol·L-1的AgNO3标准溶液滴定至终点,,测定自来水管中Cl-的含量。
①在滴定管中装入AgNO3标准溶液的前一步,应进行的操作___。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果___(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氢气从__口通入(填“a”或“b”),Y极为电池的___(填“正”或“负”)极。
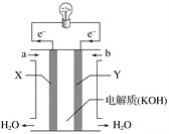
(2)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH--2e-=ZnO+H2O
Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Ag2O是__极,Zn发生__反应。
②电子由__极流向__极(填“Zn”或“Ag2O”),当电路通过0.1mol电子时,负极消耗物质的质量是___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中反应①是制备SiH4的一种方法,其副产物MgCl2·6NH3是优质的镁资源。回答下列问题:
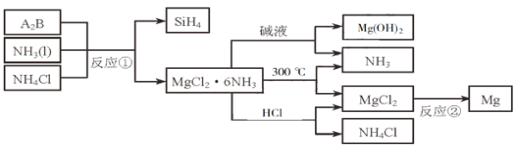
(1)MgCl2·6NH3所含元素的简单离子半径由小到大的顺序:______,Mg在元素周期表中的位置:__________,Mg(OH)2的电子式:__________。
(2)A2B的化学式为___________。上图中可以循环使用的物质有________。
(3)写出实验室制取氨气的化学方程式:______________。
(4)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料_________(写化学式)。该物质中含有的化学键类型有___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com