
| A. | 金属钠存放于煤油中 | |
| B. | 硝酸贮存在避光低温处 | |
| C. | 在盛溴的试剂瓶中加一定量的水液封,防止溴的挥发 | |
| D. | 单质碘贮存在棕色的细口瓶中 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的密度不变 | B. | 容器中压强不变 | ||
| C. | 化学平衡常数K不变 | D. | 消耗1 molA的同时生成1molB |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应除了生成新物质外,还伴随着能量的变化 | |
| B. | 有的放热反应不需要加热就能发生 | |
| C. | 焓变就是反应热,二者没有区别 | |
| D. | 化学反应是放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 适量施用化学肥料和农药 | |
| B. | 大量开采地下水,以满足社会对水的需求 | |
| C. | 减少直至不使用对大气臭氧层起破坏作用的氟氯烃 | |
| D. | 采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
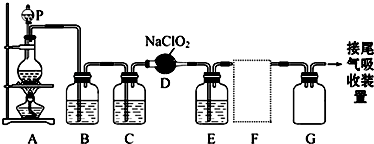

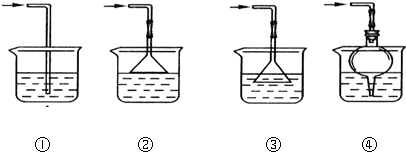
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com