
������Դ����Ľ�һ��ͻ���������Ȼ�ѧѭ��������о��ܵ��������ҵ���������
�����о����֣����������������̣�MnFe2O4��Ҳ���������Ȼ�ѧѭ���ֽ�ˮ���⣬
MnFe2O4���Ʊ��������£�

��1��Ͷ��ԭ��Fe(NO3)n��Mn(NO3)2�����ʵ���֮��ӦΪ___________��
��2��������С��������衱��Ŀ����__________________________��
��3������MnFe2O4�Ȼ�ѧѭ������ķ�Ӧ�ɱ�ʾΪ��
MnFe2O4![]() MnFe2O4��x��
MnFe2O4��x��![]() O2��
O2��
MnFe2O4��x��xH2O��MnFe2O4��xH2��
�������������������Ӧ���ش��������⣺
�� �������Ͻ�����ѭ���У�1 mol H2O���� mol H2
�� ��MnFe2O4��x��x��0.8����MnFe2O4��x��Fe2��ռȫ����Ԫ�صİٷ���Ϊ______��
�� ���MnFe2O4�Ȼ�ѧѭ��������̴��ڵIJ��㣬����Ϊ�Ȼ�ѧѭ�������Ҫ
����Ļ�ѧ������ ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ��1000K |
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��1000K |
| x |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��ʼ���� | ��ȫ���� | |
| Fe3+ | 2.7 | 4.2 |
| Mn2+ | 8.3 | 10.4 |
| 1000k |
| x |
| 2 |
| 2 |
| x |
| 2 |
| x |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ���Ĵ�ʡ�߿�ǰ�������⣨���ۣ���ѧ���� ���ͣ������
��15�֣�
������Դ����Ľ�һ��ͻ���������Ȼ�ѧѭ��������о��ܵ��������ҵ�����������о����֣����������������̣�MnFe2O4���������Ȼ�ѧѭ���ֽ�ˮ���⡣
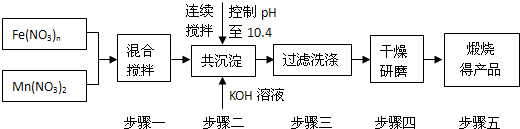
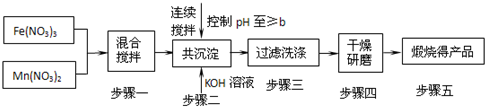
��MnFe2O4���Ʊ���
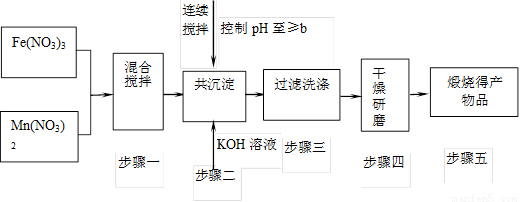

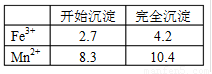
 ��֪Fe3+��Mn2+������pHΪ�±���ʾ��
��֪Fe3+��Mn2+������pHΪ�±���ʾ��
��1���˹�����������Ͷ��ԭ��Fe(NO3)3��Mn(NO3)2
 �����ʵ���֮��ӦΪ
��
�����ʵ���֮��ӦΪ
��
��2���������b��ֵΪ ��
 ��3����������ϴ�Ӹɾ��ı���
��
��3����������ϴ�Ӹɾ��ı���
��
����MnFe2O4�Ȼ�ѧѭ�����⣺
 MnFe2O4(s)��MnFe2O(4��x)(s) +
MnFe2O4(s)��MnFe2O(4��x)(s) + 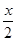 O2(g)����H1
O2(g)����H1
MnFe2O(4��x)(s)+ xH2O ��MnFe2O4(s) + xH2(g)����H2
 ��ش��������⣺
��ش��������⣺
��4�� ��MnFe2O(4��x)��x��0.8����MnFe2O(4��x)��Fe2+��ȫ����Ԫ���е���������Ϊ ��
 ��5�����Ȼ�ѧѭ��������ŵ���
������ţ���
��5�����Ȼ�ѧѭ��������ŵ���
������ţ���
A�����̼�����Ⱦ B�����Ͽ�ѭ��ʹ��  C�������������ڲ�ͬ�������ɣ���ȫ������
C�������������ڲ�ͬ�������ɣ���ȫ������
��6����֪ 2H2��g��+O2��g���� 2H2O��g������H3
 ��H3����H1����H2�Ĺ�ϵΪ��H3= ��
��H3����H1����H2�Ĺ�ϵΪ��H3= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�꼪��ʡ�߿���ϰ������⣨���ۣ���ѧ���� ���ͣ������
��15�֣�
������Դ����Ľ�һ��ͻ���������Ȼ�ѧѭ��������о��ܵ��������ҵ�������������о����֣����������������̣�MnFe2O4��Ҳ���������Ȼ�ѧѭ���ֽ�ˮ���⣬MnFe2O4���Ʊ��������£�

��1��ԭ��Fe(NO3)n��n= ��Ͷ��ԭ��Fe(NO3)n��Mn(NO3)2�����ʵ���֮��ӦΪ ��
��2��������С�������������Ŀ���� ��
��������ϴ�Ӹɾ��ı��� ��
��3������MnFe2O4�Ȼ�ѧѭ������ķ�Ӧ�ɱ�ʾΪ��
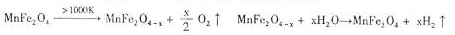
�������������������Ӧ���ش��������⣺
����MnFe2O4-x��x=0.8����MnFe2O4-x��Fe2+ռȫ����Ԫ�صİٷ���Ϊ ��
���Ȼ�ѧѭ��������ŵ��У������㼴�ɣ� ��
�۸��Ȼ�ѧѭ�����������в���֮������һ���Ľ����о������� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com