
| 步驟序号 | 操作步骤 | 现 象 |
| (1) | 用pH试纸检验 | 溶液的pH>7 |
| (2) | 向溶液中滴加氯水,再加人CC14、振荡、静置 | 下层呈橙色 |
| (3) | 向(2)所得水溶液中加人Ba(N03)2溶液和 稀 HNO3 | 有白色沉淀产生 |
| (4) | 过滤,向滤液中加人AgNO3溶液和稀HNO, | 有白色沉淀产生 |
| A. | 不能确定的离子是① | B. | 不能确定的离子是②③ | ||
| C. | 肯定含有的离子是①④⑥ | D. | 肯定没有的离子是②⑤ |
分析 (1)用pH试纸检验溶液的pH大于7,说明溶液呈碱性,应含有弱酸的酸根离子;
(2)向溶液中滴加氯水,再加入CCl4振荡,静置CCl4层呈橙色,说明溶液中含有Br-;
(3)向所得水溶液中加入Ba(NO3)2溶液和稀HNO3有白色沉淀产生,该沉淀为BaSO4,但不能确定是否含有SO42-,因SO32-可被硝酸氧化生成SO42-;
(4)过滤,向滤液中加入AgNO3溶液和稀HNO3有白色沉淀产生,该沉淀为AgCl,但不能确定溶液中是否含有Cl-,因所加氯水中含有Cl-.
解答 解:(1)用pH试纸检验溶液的pH大于7,说明溶液呈碱性,应含有弱酸的酸根离子,该离子只能为SO32-,则溶液中一定不存在Ba2+,因二者能生成沉淀而不能大量共存,
一定含有Na+,根据溶液呈电中性原则,阳离子只有Na+;
(2)向溶液中滴加氯水,再加入CCl4振荡,静置CCl4层呈橙色,说明溶液中含有Br-;
(3)向所得水溶液中加入Ba(NO3)2溶液和稀HNO3有白色沉淀产生,该沉淀为BaSO4,但不能确定是否含有SO42-,因SO32-可被硝酸氧化生成SO42-;
(4)过滤,向滤液中加入AgNO3溶液和稀HNO3有白色沉淀产生,该沉淀为AgCl,但不能确定溶液中是否含有Cl-,因所加氯水中含有Cl-.
由以上分析可知,溶液中一定含有的离子为①④⑥,可能含有的离子为③⑤,一定不存在的是②.
故选C.
点评 本题考查离子反应及离子组成分的判断,题目难度不大,本题注意把握离子的性质及离子共存问题.


科目:高中化学 来源: 题型:选择题
| A. | 用新制Cu(OH)2悬浊液检验乙醛:向10ml10%的硫酸铜溶液中加的2%NaOH溶液4-6滴,振荡后加入乙醛溶液0.5ml,加热 | |
| B. | 探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象 | |
| C. | 向盛有过量苯酚浓溶液的试管里逐滴加入稀溴水,边加边振荡,观察三溴苯酚的生成 | |
| D. | 提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入过量饱和氢氧化钠溶液,振荡后静置分液,并除去有机层的水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.| 实验序号 | 温度/℃ | 各物质的体积/mL | 反应时间 | |||
| H2O | 3mol/L稀硫酸 | 0.1mol/L KMnO4溶液 | 0.6mol/LH2C2O4溶液 | |||
| 1 | 25 | 3.0 | 2.0 | 4.0 | 6.0 | t1 |
| 2 | 25 | ① | 2.0 | 4.0 | 4.0 | t2 |
| 3 | ② | 7.0 | 2.0 | 4.0 | 2.0 | t3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
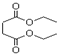
| A. | 1mol琥珀酸二乙酯能与4mol的NaOH反应 | |
| B. | 琥珀酸二乙酯在一定条件下能发生取代、加成和氧化反应 | |
| C. | 琥珀酸的分子式为C4H8O4 | |
| D. | 琥珀酸分子中含有六元环 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
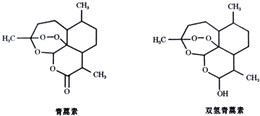
| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 青蒿素和双氢青蒿素不是同分异构体 | |
| C. | 青蒿素和双氢青蒿素都能发生酯化反应 | |
| D. | 青蒿素在稀硫酸催化条件下能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 78 g Na2O2中存在的共价键总数为NA | |
| B. | 0.1 mol${\;}_{38}^{90}$Sr原子中含中子数为3.8NA | |
| C. | 氢氧燃料电池负极消耗2.24 L气体时,电路中转移的电子数为0.1NA | |
| D. | 0.1 mol氯化铁溶于1L水中,所得溶液中Fe3+的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,1L pH=3的硫酸溶液中,SO42-离子的数目约为5×10-4NA | |
| B. | 1mol氨基(NH2)中含有电子的数目为10NA | |
| C. | 一定条件下,1molN2与3molH2充分反应,转移电子的数目可能为2NA | |
| D. | 3molNO2和H2O完全反应,被还原的NO2分子数目为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32g | |
| B. | 1 molNa2O2固体中含离子总数为4NA | |
| C. | 1mol羟基与17gNH3所含电子数之比为9:10 | |
| D. | 1molNa2CO3晶体中含CO32-离子数小于NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com