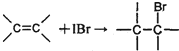�������A��B��С�⣬�ֱ��Ӧ�ڡ����ʽṹ�����ʡ��͡�ʵ�黯ѧ������ѡ��ģ������ݣ���ѡ������һ�⣬������Ӧ�Ĵ������������������ⶼ������A�����֣�
A����1��K
3[Fe��CN��
6]���軯���ֽг�Ѫ�Σ������ɫб�����壬������ˮ����������ζ��������ˮ����ͪ���������Ҵ���
�ٷ����ڲ�����
CEF
CEF
������ţ���
A�����Ӽ� B�����Լ� C��������D����λ�� E����� F���Ǽ��Լ�
���������ӵĻ�̬�����Ų�ʽ
[Ar]3d5
[Ar]3d5
��
�����CN
-�ĵȵ�������
CO��N2
CO��N2
��д�����֣���
���ü۵��ӶԻ������ۿ�֪�����������ӵĿռ乹��Ϊ
V��
V��
��
��2����Ԫ�����ﱡĤ̫���ܵ�ز���Ϊ���Σ�����Ҫ�����黯�ء����ӡ���п��ͭ������Ĥ��صȣ�
�ٵ�һ�����ܣ�As
��
��
Se�����������������=������
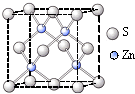
����п�ľ����У��ṹ����ͼ��ʾ���������ӵ���λ����
4
4
��
B��ij��ѧ�о���ѧϰС��Ϊ̽��ijƷ�ƻ������в�����֬����ĺ���������������ʵ�飺
����I����ȡ0.4g��������Ʒ��������������ĵ�ƿ����ͼ���ڣ�����10mL���Ȼ�̼������ҡ��ʹ��ȫ���ܽ⣮���ƿ�м���25.00mL��0.01mol IBr����ˮ������Һ���Ǻ�ƿ�����ڲ�������ƿ��֮��μ�����10%�⻯����Һ��շ�϶������IBr�Ļӷ���ʧ��
����II���ڰ�������30min������ʱ����ҡ����30min��С�ĵش��������������Ƶ�10%�⻯��10mL������ˮ50mL�Ѳ�������ƿ���ϵ�Һ���ϴ��ƿ�ڣ�
�������ָʾ������0.1mol?L
-1�����������Һ�ζ���������ƿ��ֱ���յ㣮
�ⶨ�����з�������ط�Ӧ���£�

��
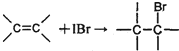
��IBr+KI=I
2+KBr
��I
2+2S
2O
32-=2I
-+S
4O
62-��ش��������⣺
��1����֪±�ػ�����IBr��������±�ص������ƣ�ʵ����ȷ��ȡIBr��ҺӦѡ�õ�������
��ʽ�ζ���
��ʽ�ζ���
����ƿ������ᷢ����Ӧ�Ļ�ѧ����ʽ
IBr+H2O=HIO+HBr
IBr+H2O=HIO+HBr
��
��2��������е�ƿ�ڰ�������30min������ʱ����ҡ����ԭ����
��ƿ���ڰ����ɼ����廯��ӷ������Ͻ������������ʼ��ַ�Ӧ
��ƿ���ڰ����ɼ����廯��ӷ������Ͻ������������ʼ��ַ�Ӧ
��
��3�������������ָʾ��Ϊ
������Һ
������Һ
���ζ��յ������
��Һ����ɫǡ�ñ�Ϊ��ɫ��30���ڲ��仯
��Һ����ɫǡ�ñ�Ϊ��ɫ��30���ڲ��仯
��



 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�