
| A. | MgBr2 | B. | Na2S | C. | KI | D. | KCl |
分析 与氖原子核外电子排布相同的离子有:N3-、O2-、F-、Na+、Mg2+、Al3+,跟氩原子核外电子排布相同的离子有P3-、S2-、Cl-、K+、Ca2+,据此分析解答.
解答 解:与氖原子核外电子排布相同的离子有:N3-、O2-、F-、Na+、Mg2+、Al3+,跟氩原子核外电子排布相同的离子有P3-、S2-、Cl-、K+、Ca2+,
A.Mg2+和Ne核外电子排布式相同、Br-和Ar原子核外电子排布式不相同,所以不符合条件,故A错误;
B.Na+与Ne原子核外电子排布式相同,S2-和Ar原子核外电子排布式相同,所以符合条件,故B正确;
C.Na+与Ne原子核外电子排布式相同,I-和Ar原子核外电子排布式不相同,所以不符合条件,故C错误;
D.Cl-、K+和Ar原子核外电子排布式相同,不符合条件,故D错误;
故选B.
点评 本题考查了离子核外电子排布式,明确形成10电子、18电子简单离子有哪些是解本题关键,根据离子是否符合题意即可,题目难度不大.


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:解答题

| 序号 | 实验步骤 | 简述实验操作(不必叙述如何组装实验装置) |
| ① | 溶解 | 将混合物放入烧杯中,加入热的蒸馏水,充分搅拌直到固体不再溶解. |
| ② | ||
| ③ | ||
| ④ | ||
| ⑤ | 过滤、干燥 | 得到K2Cr2O7晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
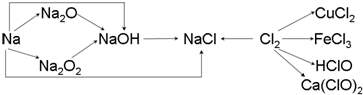
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称取8g NaOH固体放入烧杯中,加入100 mL蒸馏水,并不断搅拌至固体溶解 | |
| B. | 称取8g NaOH固体,放入100 mL容量瓶中,加入蒸馏水使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 | |
| C. | 称取8 g NaOH固体,放入100 mL量筒中,加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100 mL | |
| D. | 称取8g NaOH固体放入烧杯中,加入适量蒸馏水溶解,冷却后将烧杯中溶液注入100 mL容量瓶后,用少量蒸馏水洗涤烧杯内壁2~3次 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱金属单质在化学反应中表现出强还原性 | |
| B. | Li 在氧气中燃烧主要生成Li2O2 | |
| C. | 碱金属离子的氧化性随着离子半径的增大而减小 | |
| D. | 随核电荷数的增加,单质与水反应剧烈程度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y和Z互为同位素 | |
| B. | X和Y能化合成两种化合物 | |
| C. | X和Y化合的产物中一定不含有共价键 | |
| D. | X离子比R的离子半径大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 $\stackrel{②}{→}$X$→_{③△}^{NaOH乙醇溶液}$乙
$\stackrel{②}{→}$X$→_{③△}^{NaOH乙醇溶液}$乙 .
. ).写出同时符合下列要求的丙的同分异构体结构简式
).写出同时符合下列要求的丙的同分异构体结构简式 、
、 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com