
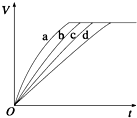
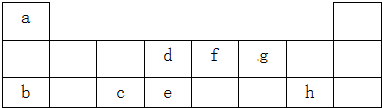
 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实验条件,下列说法中一定不正确的是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实验条件,下列说法中一定不正确的是( ) | 组别 | 对应曲线 | c(HCl)/mol•L-1 | 反应温度/℃ | 铁的状态 |
| 1 | a | 30 | 粉末状 | |
| 2 | b | 30 | 粉末状 | |
| 3 | c | 2.5 | 块状 | |
| 4 | d | 2.5 | 30 | 块状 |
| A. | 第4组实验的反应速率最慢 | |
| B. | 第1组实验中盐酸的浓度大于2.5 mol•L-1 | |
| C. | 第2组实验中盐酸的浓度等于2.5 mol•L-1 | |
| D. | 第3组实验的反应温度低于30℃ |
分析 相同时间内生成氢气的体积越大,说明反应速率越快,由图可知,反应速率a>b>c>d,根据外界条件(浓度、温度、压强、催化剂、固体表面积)对化学反应速率的影响进行分析.
解答 解:相同时间内生成氢气的体积越大,说明反应速率越快,由图可知,反应速率a>b>c>d,
A.由图可知,相同时间内,曲线d生成的氢气的体积最少,故第4组实验的反应速率最慢,故A正确;
B.第1组反应速率比第4组快,1、4组相比,温度相同,1组固体表面积更大,故第1组盐酸的浓度可能等于、小于或大于2.5mol•L-1,故B正确;
C.第2组反应速率比第4组快,2、4组相比,温度相同,2组固体表面积更大,故第2组盐酸的浓度可能等于、小于或大于2.5mol•L-1,故C正确;
D.第3组反应速率比第4组快,3、4组相比,浓度、固体表面积相同,温度越高反应速率越快,故第3组实验的反应温度高于30℃,故D错误;
故选D.
点评 本题考查铁等质量时,探究盐酸浓度、反应温度、铁的颗粒大小不同对化学反应速率的影响,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③⑥ | C. | ④⑤⑥ | D. | ①⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入氩气,V正、V逆都增大,且V正增大倍数大于V逆增大倍数 | |
| B. | 加入催化剂,V正、V逆都发生变化,且变化的倍数相同 | |
| C. | 增大压强时,V正、V逆都增大,且V正增大倍数大于V逆增大倍数 | |
| D. | 降低温度时,V正、V逆都减小,且V正减小倍数小于V逆减小倍数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 | |
| B. | 棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O | |
| C. | 植物油和裂化汽油可用溴水鉴别 | |
| D. | 在鸡蛋白溶液中加入浓HNO3,微热后会生成黄色物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某元素基态原子的电子排布图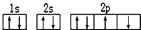 | |
| B. | NH4Cl电子式为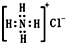 | |
| C. | Ca2+离子基态电子排布式为1s22s22p63s23p6 | |
| D. | 钾(K)的原子结构示意图为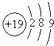 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
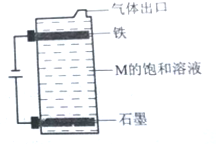 A、B、C、D、E为原子序数依次增大的短周期元素.A、C处于同一主族,C、D、E处于同一周期;A、B组成的气体X能使湿润的红色石蕊试纸变蓝.C在短周期元素中金属性最强,E原子的最外层电子数是A、B、C原子最外层电子数之和,E的单质与x反应能生成溶于水呈强酸性的化合物Z,同时生成B的单质,D的单质既能与C的最高价氧化物的水溶液反应,也能与Z的水溶液反应;C、E可组成化合物M.
A、B、C、D、E为原子序数依次增大的短周期元素.A、C处于同一主族,C、D、E处于同一周期;A、B组成的气体X能使湿润的红色石蕊试纸变蓝.C在短周期元素中金属性最强,E原子的最外层电子数是A、B、C原子最外层电子数之和,E的单质与x反应能生成溶于水呈强酸性的化合物Z,同时生成B的单质,D的单质既能与C的最高价氧化物的水溶液反应,也能与Z的水溶液反应;C、E可组成化合物M. .
.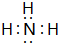 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com