
| A. | 镁单质能和冷水发生剧烈的反应 | B. | 碱性Mg(OH)2<Al(OH)3 | ||
| C. | 稳定性SiH4<HCl | D. | 金属性Na<Mg |
分析 A.金属性越强,与水反应越剧烈;
B.金属性越强,对应碱的碱性越强;
C.非金属性越强,对应氢化物越稳定;
D.同周期从左向右金属性减弱.
解答 解:A.金属性越强,与水反应越剧烈,Na与冷水反应,而Mg不能与冷水剧烈反应,故A错误;
B.金属性Mg>Al,对应碱的碱性为Mg(OH)2>Al(OH)3,故B错误;
C.非金属性Cl>Si,对应氢化物的稳定性为SiH4<HCl,故C正确;
D.同周期从左向右金属性减弱,则金属性Na>Mg,故D错误;
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 钠和镁分别与冷水反应,判断金属性强弱 | |
| B. | 在MgCl2与AlCl3溶液中分别加入过量氨水,判断Mg与Al的金属性强弱 | |
| C. | 硅酸钠溶液中通入CO2气体,判断碳与硅的非金属性强弱 | |
| D. | Br2与I2分别与足量H2反应,判断溴与碘的非金属性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
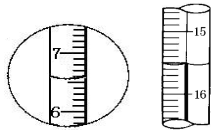
| A. | 左边是量筒读数6.5mL,右边是滴定管读数16.50mL | |
| B. | 左边是量筒读数7.5mL,右边是滴定管读数16.50mL | |
| C. | 左边是量筒读数6.5mL,右边是滴定管读数15.50mL | |
| D. | 左边是量简读数6.5mL,右边是滴定管读数16.50mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g)?2C(g)△H<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2,下列有关说法正确的是( )
一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g)?2C(g)△H<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2,下列有关说法正确的是( )| A. | 反应开始2min内,v(A)=0.025mol/(L•mol) | |
| B. | t1时改变的条件可能是升高温度 | |
| C. | t3时改变的条件可能是加压,此时c(B)不变 | |
| D. | t4时可能是使用了催化剂,此时c(B)不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子数不同 | B. | 质子数相同 | C. | 氧原子数相同 | D. | 气体质量相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com