
| A. | X的电负性大于Y的电负性 | B. | X的原子半径大于Y的原子半径 | ||
| C. | X的氧化性大于Y的氧化性 | D. | X的第一电离能大于Y的第二电离能 |
分析 X元素的阴离子和Y元素的阳离子具有相同的电子层结构,离子核外电子数目相等,则Y元素处于X元素的下一周期,X为非金属元素,最外层电子数较多,Y为金属元素,最外层电子数相对较少.
解答 解:X元素的印离子和Y元素的阳离子具有相同的电子层结构,离子核外电子数目相等,则Y元素处于X元素的下一周期,X为非金属元素,最外层电子数较多,Y为金属元素,最外层电子数相对较少,
A、X为非金属元素,Y为金属元素,故X的电负性高于Y的电负性,故A正确;
B、Y元素处于X元素的下一周期,X为非金属元素,原子半径小于同周期与Y处于同族的元素,故原子半径Y>X,故B错误;
C、X为非金属元素,Y为金属元素,故X的氧化性强于Y的氧化性,故C正确;
D、X为非金属元素,Y为金属元素,故X的第一电离能大于Y的第一电离能,故D正确;
故选B.
点评 本题考查结构与位置的关系、半径与电负性、第一电离能比较等,难度不大,关键根据离子具有相同的电子层结构推断元素的相对位置.


科目:高中化学 来源: 题型:解答题
| 元素 | 有关信息 |
| X | 在元素周期表中原子半径最小 |
| Y | 最外层电子数是次外层的2倍 |
| Z | 元素的主要合价为一2价 |
| M | 其单质及化合物的焰色反应呈黄色 |
| N | 与Y同主族,其单质为半导体 |
 ;M2Z中所含化学键类型是离子键.
;M2Z中所含化学键类型是离子键.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
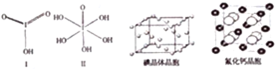
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氯、晶体硅、臭氧均属于单质 | B. | 盐酸、醋酸、苯酚均属于强电解质 | ||
| C. | CO2、CCl4、蛋白质均属于有机物 | D. | CuO、MgO、Na2O2均属于碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分馏石油获得汽油、煤油和柴油 | |
| B. | 干馏煤获得焦炉煤气、煤焦油和焦炭 | |
| C. | 以煤、石油和天然气为原料生产合成材料 | |
| D. | 从海水中提取溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂的水解产物为葡萄糖 | B. | 蔗糖水解的最终产物是葡萄糖 | ||
| C. | 常温下,淀粉遇碘变蓝色 | D. | 蛋白质烧焦时没有特殊气味 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
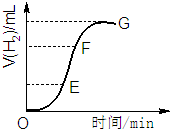 用不纯的锌粒与2mol/L盐酸反应制取氢气气体,请回答:
用不纯的锌粒与2mol/L盐酸反应制取氢气气体,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
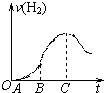
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com