
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知:CH4(g)+H2O(g)====CO(g)+3H2(g) ΔH=206.2 kJ·mol-1
CH4(g)+CO2(g)====2CO(g)+2H2(g) ΔH=247.4 kJ·mol-1
2H2S(g)====2H2(g)+S2(g) ΔH=169.8 kJ·mol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为_______________________。
(2)H2S热分解制氢时,常向反应器中通入一定比例的空气,使部分H2S燃烧,其目的是___________________________ _______________________________;
_______________________________;
燃烧生成的SO2与H2S进一步反应,生成物在常温下均不是气体,写出该反应的化学方程式:_______________________________________。
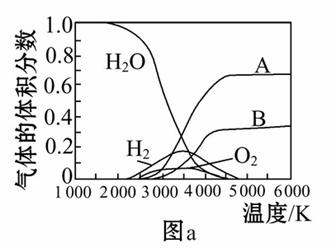
(3)H2O的热分解也可得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如图a所示。图中A、B表示的物质依次是________________________。
(1)将反应标号:
①CH4(g)+H2O(g)====CO(g)+3H2(g) ΔH=206.2 kJ·mol-1;
②CH4(g)+CO2(g)====2CO(g)+2H2(g) ΔH=247.4 kJ·mol-1
③2H2S(g)====2H2(g)+S2(g) ΔH=169.8 kJ·mol-1
则反应CH4(g)+2H2O(g)====CO2(g)+4H2(g)可以由①×2-②得到,ΔH=206.2×2-247.4=165.0 (kJ·mol-1)。
(2)H2S的热分解需要能量来引发,H2S的燃烧为放热反应,可以为分解提供能量。
(3)水在2 000 K左右可以分解为氢气、氧气;当温度继续升高,氢气、氧气也获得了足够的能量继续分解为氢原子、氧原子。
(4)电解尿素,阳极区为失去电子的氧化反应,生成氮气。
(5)根据“仅含一种金属元素的氢化物(其中氢的质量分数为0.077)”,假设仅含一个氢原子,则M=1/0.077≈13,金属的相对原子质量=13-1=12,舍掉;假设含有两个氢原子,M=2/0.077≈26,金属的相对原子质量=26-2=24,可得该金属氢化物为MgH2。
答案:(1)CH4(g)+2H2O(g)==== CO2(g)+4H2(g) ΔH=165.0 kJ·mol-1
(2)为H2S热分解反应提供热量
2H2S+SO2====2H2O+3S(或4H2S+2SO2====4H2O +3S2)
+3S2)
(3)H、O(或氢原子、氧原子)
(4)CO(NH2)2+8OH--6e-====CO32-+N2↑+6H2O
(5)2Mg2Cu+3H2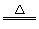 MgCu2+3MgH2
MgCu2+3MgH2
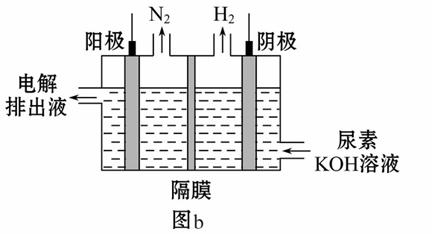
(4)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见图b(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为______。
(5)Mg2Cu是一种储氢合金。350 ℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077)。Mg2Cu与H2反应的化学方程式为__________________。


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
下列有关实验装置进行的相应实验,不能达到实验目的的是 ( )
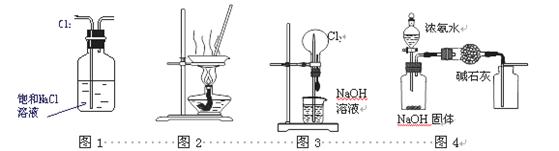
A.用图1所示装置除去Cl2中含有的少量HCl
B.用图2所示装置蒸发KCl溶液制备无水KCl
C.用图3所示装置可以完成“喷泉”实验
D.用图4所示装置制取干燥纯净的NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于实验现象的描述不正确的是( )
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.用锌片作负极,铜片作正极,在CuSO4溶液中,铜片质量增加
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出的速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生用如图所示装置进行化学反应X+2Y====
2Z能量变化情况的研究。当往试管中滴加试剂Y时,看到导管中甲处液面下降,乙处液面上升。关于该反应的叙述正确的是( )
①该反应为放热反应
②生成物的总能量比反应物的总能量高
③该反应过程可以看成是“贮存”于X、Y内部的能量转化为热量而释放出来
A.①②③ B.①③
C.①② D.②
查看答案和解析>>
科目:高中化学 来源: 题型:
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为:
xMg+Mo3S4 MgxMo3S4
MgxMo3S4
在镁原电池放电时,下列说法错误的是( )
A.Mg2+向正极迁移
B.正极反应为Mo3S4+2xe-====Mo3S42x-
C.Mo3S4发生氧化反应
D.负极反应为xMg-2xe-====xMg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,通过下列反应可实 现燃煤烟气中硫的回收:
现燃煤烟气中硫的回收:
SO2(g)+2CO(g) 2CO2(g)+S(l) ΔH<0
2CO2(g)+S(l) ΔH<0
若反应在恒容的密闭容器中 进行,下列有关说法正确的是( )
进行,下列有关说法正确的是( )
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应的平衡常数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)  2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),据此得出的结论不正确的是( )
2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),据此得出的结论不正确的是( )
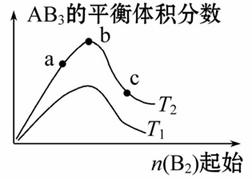
A.达到平衡时A2的转化率大小为b>a
B.a、b、c三点的平衡常数相同
C.若T2>T1,则正反应一定是吸热反应
D.b点时,平衡体系中A、B原子数之比一定是1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
比较等物质的量浓度的:①H2SO3;②NaHSO3;③Na2SO3。三种溶液中[SO32-]的大小,排列正确的是( )
A.①>②>③ B.③>②>①
C.②>①>③ D.③>①>②
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H2(g)+I2(g)2HI(g) ΔH<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2 mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是
( )
A.甲、乙提高相同温度
B.甲中加入0.1 mol He,乙不变
C.甲降低温度,乙不变
D.甲增加0.1 mol H2,乙增加0.1 mol I2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com