

 ,反应类型加聚反应;
,反应类型加聚反应;
 .
. 分析 (1)①乙烯和溴能发生加成反应生成1,2-二溴乙烷;
②乙烯能发生加聚反应生成聚乙烯;
③一定条件下,乙烯能和水发生加成反应生成乙醇;
④乙烯能燃烧生成二氧化碳和水;
(2)①丙烯发生加聚反应生成聚丙烯;
②2-丁烯含有碳碳双键,在一定条件下发生反应生成聚2-丁烯.
解答 解:(1)①乙烯和溴能发生加成反应生成1,2-二溴乙烷,反应方程式为:CH2=CH2+Br2→CH2BrCH2Br;该反应的反应类型是加成反应,
故答案为:CH2=CH2+Br2→CH2Br-CH2Br;加成反应;
②、乙烯能发生加聚反应生成聚乙烯,反应方程式为:nCH2=CH2$\stackrel{一定条件}{→}$ ;该反应的反应类型是加聚反应,
;该反应的反应类型是加聚反应,
故答案为:nCH2=CH2$\stackrel{一定条件}{→}$ ;加聚反应;
;加聚反应;
③一定条件下,乙烯能和水发生加成反应生成乙醇,反应方程式为CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,
故答案为:CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH;
④乙烯能燃烧生成二氧化碳和水,反应方程式为:CH2=CH2+3O2$\stackrel{点燃}{→}$2CO2+2H2O,
故答案为:CH2=CH2+3O2$\stackrel{点燃}{→}$2CO2+2H2O;
(2)①丙烯发生加聚反应生成聚丙烯,化学方程式为: ,
,
故答案为: ;
;
②2-丁烯在催化剂作用下生成聚2-丁烯反应的化学方程式为: ;
;
故答案为: .
.
点评 本题考查有机物的机构和性质,为高考常见题型,注意把握有机物的官能团的性质以及相关方程式的书写,为解答该题的关键,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 大于52% | B. | 等于52% | C. | 小于52% | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入稀盐酸产生无色气体,原物质一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入稀盐酸后再加入硝酸银,产生白色沉淀,则原溶液一定有Cl- | |
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,不一定有Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
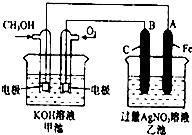 如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O 填写下列空白:
如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O 填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定含有SO42- | B. | 一定含有Ag+ | ||
| C. | 可能不含CO32- | D. | 可能含有SO42-或Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com