
����Ŀ����֪Ksp(AgCl)=1.8��10-10��Ksp(AgI)=1.0��10-16�����й���������֮��ת����˵���д������( )
A.AgCl������ˮ������ת��ΪAgI
B.�����������Ksp���Խ���������Խ����ת��Ϊ�����ܵ�����
C.AgI��AgCl��������ˮ������AgCl����ת��ΪAgI
D.�����£�AgCl��Ҫ��NaI��Һ�п�ʼת��ΪAgI����NaI��Ũ�ȱ��벻����![]()
 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д� ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ʵĵ���ƽ�ⳣ�������
������� | HCOOH | HCN |
|
|
����ƽ�ⳣ�� |
|
|
|
|
����˵���������![]()
A.���![]() ��������
��������![]()
B.![]() ��
��![]() ��Һ�д������¹�ϵʽ��
��Һ�д������¹�ϵʽ��![]()
C.![]() ��������
��������![]() �İ�ˮ��ϣ�����Һ�����ԣ���
�İ�ˮ��ϣ�����Һ�����ԣ���![]() ����
����![]() ��ˮ
��ˮ![]()
D.���������Ũ�ȵ�HCOONa��NaCN
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС��������ϣ��������������֤ SO2 �Ļ�ԭ�ԡ�

��֪������ D ϴ�Ӹɾ��������������ʱ�����ֳ����ܽ⣬ʣ���������� F��(1)��������ɫ���� B���ijɷ�
����ͬѧ�ƶϰ�ɫ���� B �� Ag2SO4��
ʵ���������ݣ������� F��˵�������� D���к�________________ (�ѧʽ)������˵������ɫ����B���к� Ag2SO4��
����ͬѧ��Ϊ����ɫ���� B���к��� Ag2SO3��
ʵ���������ݣ������� D ϴ�Ӹɾ��������������ʱ�����ֳ����ܽ������ܽ������Ϊ BaSO3�� �����ƶϳ��� B �к� Ag2SO3��Ϊ��һ��֤ʵ B �к��� Ag2SO3����ȡ������Һ E���Թ��м�������________________���а�ɫ�������ɡ�
(2)�����£�Ag2SO4 �� Ag2SO3 �� c(Ag+)�� c(SO32-)�Ĺ�ϵ����ͼ��ʾ��
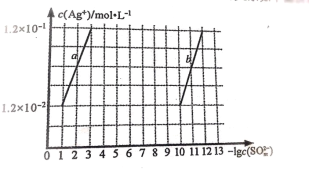
��֪��Ksp(Ag2SO4)��Ksp(Ag2SO3)���ش����⣺
����ʾ Ag2SO4 �ij����ܽ�ƽ���ϵ��������________________ (����a������b��)
��Ksp(Ag2SO3)Ϊ________________mol3L-3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ��ԭ���������۾���ȷ���ǣ� ��
A.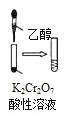 ͼ�еμ��Ҵ����Թ��г�ɫ��Һ��Ϊ��ɫ��˵��
ͼ�еμ��Ҵ����Թ��г�ɫ��Һ��Ϊ��ɫ��˵��![]() ����ԭ��
����ԭ��![]()
B.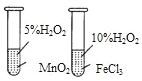 ͼ�У��ұ��Թ��в�������Ѹ�٣�˵���Ȼ����Ĵ�Ч���ȶ������̺�
ͼ�У��ұ��Թ��в�������Ѹ�٣�˵���Ȼ����Ĵ�Ч���ȶ������̺�
C.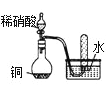 ͼ�У����Թ����ռ�������ɫ���壬֤��ͭ��ϡ����ķ�Ӧ������NO
ͼ�У����Թ����ռ�������ɫ���壬֤��ͭ��ϡ����ķ�Ӧ������NO
D.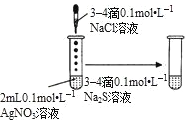 ͼ�У��Թ����ȳ��ְ�ɫ��������
ͼ�У��Թ����ȳ��ְ�ɫ��������![]() �������ɫ��������������֤AgCl���ܽ�ȴ���
�������ɫ��������������֤AgCl���ܽ�ȴ���![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ���¶Ⱥ�ѹǿ�Է�ӦX��Y![]() 2ZӰ���ʾ��ͼ��ͼ�к������ʾ�¶ȣ��������ʾƽ����������Z���������������������ȷ���ǣ� ��
2ZӰ���ʾ��ͼ��ͼ�к������ʾ�¶ȣ��������ʾƽ����������Z���������������������ȷ���ǣ� ��
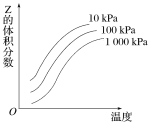
A.�������淴Ӧ������ӦΪ���ȷ�ӦB.X��Y��Z��Ϊ��̬
C.X��Y�����ֻ��һ��Ϊ��̬��ZΪ��̬D.������Ӧ���淴Ӧ����H��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ѱ۳����ᣨ��Ҫ�����ᡢFe3+��Fe2+��TiO2+��Al3+���Ʊ����������[(NH4)2S2O8]��ͬʱ����TiO(OH)2�ļ�Ҫ�������£�
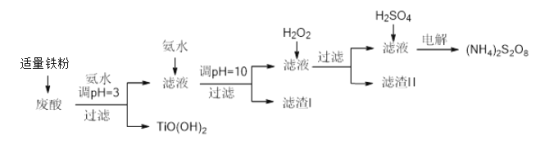
��֪��i.����������ȫ�����������������pH��
�������� | TiO2+ | Fe3+ | Fe2+ | Al3+ |
��ʼ������PH | 1.2 | 1.9 | 7.0 | 3.2 |
������ȫ��pH | 2.8 | 3.1 | 9.4 | 4.7 |
ii.pH>7ʱ��Fe2+��������Fe(II)��������[Fe(NH3)2]2+��
��ش��������⣺
��1��������������������________________________��
��2������TiO(OH)2�Ļ�ѧ����ʽ��____________________��
��3������I���������о����е����ʵĻ�ѧʽ��________
��4������H2O2��Ŀ������������Fe(II)��������[Fe(NH3)2]2+����ƽ�������ӷ���ʽ��2[Fe(NH3)2]2++____________+4H2O +H2O2=___________+ 4NH3��H2O��
��5�������£����Һ�к�������Ҫ������ʽ��pH�Ĺ�ϵ����ͼ��ʾ��
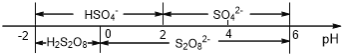
�������ŵ��������ҪΪHSO4-���������������Һ��pH��ΧΪ_________
��6����֪Ksp[Al(OH)3]=3.2��10-34 ����pH=10 ʱ������Һ��c(Al3+)=___________
��7��25�棬pH=3��(NH4)2SO4��Һ�У�����2c(SO42-)- c(NH4+) =___________����ʽ���ɣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����������Ԫ�ص����� aA2+��bB+��cC3-��dD-��������ͬ�ĵ��Ӳ�ṹ������������ȷ����
A.���ӵĻ�ԭ�ԣ�C3-<D-B.���Ӱ뾶��C>D>B>A
C.ԭ�������� d>c>b>aD.���ʵĻ�ԭ�ԣ� A>B>D>C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������ʽṹ�����ʵ�˵����ȷ����
A.����£�22.4 L C2H2����������������18 g�����������������Ϊ2NA
B.�������������NH3��H2O��HF�ķе㷴�����Ҹߵ�˳��ΪHF��H2O��NH3
C.VSEPRģ�;��Ƿ��ӵĿռ乹��
D.HF��HCl��HBr��HI�����ȶ��Ժͻ�ԭ�Դ��������μ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���![]() ����ͨ��100mLˮ�������ͣ�Ȼ�������ñ�����ˮ����μ���
����ͨ��100mLˮ�������ͣ�Ȼ�������ñ�����ˮ����μ���![]() ��Һ������������pH�ı仯��ͼ��ʾ�������й�������ȷ����( )
��Һ������������pH�ı仯��ͼ��ʾ�������й�������ȷ����( )
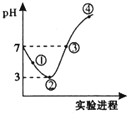
A.���ߢۢܶ������ӷ�Ӧ��![]()
B.�����ݢڴ����ݼ������ܽ��![]()
C.�۴���ʾ����������������Һǡ�÷�Ӧ��ȫ
D.�ٴ�![]() ԼΪ
ԼΪ![]() ��
��![]() ������
������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com