
| A. | 裂化和裂解产物中都含有不饱和烃 | |
| B. | 裂解和裂化都是为了得到气态烃 | |
| C. | 裂解和裂化的温度不同 | |
| D. | 裂化和裂解都是使相对分子质量大的烃断裂为相对分子质量小的烃的过程 |
分析 A.石油裂化和裂解都可以得到不饱和烃;
B.结合石油裂化的目的和裂解的目的不同分析判断;
C.裂解与裂化的温度不同;
D.裂化和裂解都是由一种大分子的烃在高温无氧下变成小分子烃的复杂分解反应的过程.
解答 解:A.石油裂化和裂解产物为烷烃和烯烃,产物中都含有不饱和烃,故A正确;
B.石油裂化的目的是为了提高轻质液体燃料(汽油,煤油,柴油等)的产量,特别是提高汽油的产量,裂解的目的是为了获得乙烯、丙烯、丁二烯、丁烯、乙炔等,故B错误;
C.裂解与裂化的原料都是石油分馏产品如原油或重油等,发生反应的温度不同,故C正确;
D.裂化和裂解都是由一种大分子的烃在高温无氧下变成小分子烃的复杂分解反应的过程,故D正确.
故选B.
点评 本题考查裂化和裂解的原理和产物,题目难度不大,注意裂解石油裂化和裂解都可以得到不饱和烃.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 单质分子中均不存在化学键 | |
| C. | 含有分子间作用力的分子一定含有共价键 | |
| D. | 离子化合物中一定含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠的取用量不足 | |
| B. | 钠的取用量过量 | |
| C. | 采用20℃、1.01×105Pa的V(H2)进行最终的计算 | |
| D. | 仰视读取测水体积的量筒的刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,C中官能团的名称为 羧基.
,C中官能团的名称为 羧基. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 )有下列叙述:①不能使酸性KMnO4溶液褪色;②能使溴的四氯化碳溶液褪色;③不可溶于水;④可溶于苯中;⑤能与浓硝酸发生取代反应;⑥所有的原子不可能共平面.其中正确的是( )
)有下列叙述:①不能使酸性KMnO4溶液褪色;②能使溴的四氯化碳溶液褪色;③不可溶于水;④可溶于苯中;⑤能与浓硝酸发生取代反应;⑥所有的原子不可能共平面.其中正确的是( )| A. | ②③④⑤ | B. | ①②⑤⑥ | C. | ①②④⑤⑥ | D. | 全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 短周期元素X、Y的价电子数相同,且原子序数比等于$\frac{1}{2}$;元素Z位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.
短周期元素X、Y的价电子数相同,且原子序数比等于$\frac{1}{2}$;元素Z位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
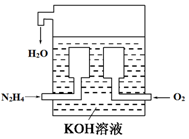
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
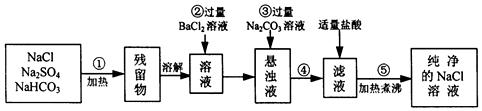
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com