
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.Na2O2与Na2O | B.Na和NaOH | C.Na2O2和Na | D.Na和Na2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.①③ | C.②③ | D.①②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 ,加入试剂的合理顺序为 (选填a,b,c多选扣分)
,加入试剂的合理顺序为 (选填a,b,c多选扣分)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 合并配成溶液,向溶液中滴加0.1mol·L--1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2
合并配成溶液,向溶液中滴加0.1mol·L--1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2 的物质的量的关系是
的物质的量的关系是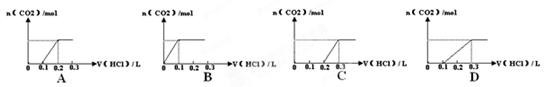
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
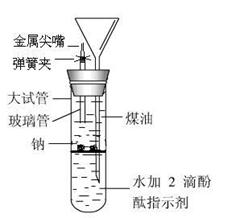
 ;
;查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 l·L-1 NaOH溶液480 mL。配制方法如下:
l·L-1 NaOH溶液480 mL。配制方法如下: 溶液混合均匀;
溶液混合均匀;| A.所用的NaOH中混有少量Na2O |
| B.用托盘天平称量一定质量固体NaOH时,所用的小烧杯内壁不太干燥 |
| C.配制溶液所用的容量瓶洗净后没有烘干 |
| D.固体NaOH在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com