
在氯化铁、氯化铜和盐酸的混合溶液中加入铁粉,待反应结束后,所剩余的固体滤出后能被磁铁吸引,反应后溶液存在较多的阳离子是 ( )
A.Cu2+ B.Fe3+ C.Fe2+ D.H+
科目:高中化学 来源: 题型:
菱锰矿的主要成分是MnCO3(含有少量FeS2、Al2O3),以菱锰矿为原料制备锰单质的流程如下所示:

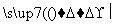 浆化
浆化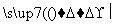 溶液1
溶液1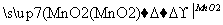 溶液2
溶液2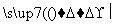 精制—→电解—→Mn
精制—→电解—→Mn
请回答下列问题:
(1)菱锰矿在浸取前需要粉碎,其目的是______________________________。
(2)用稀硫酸浸取时,主要反应的离子方程式为____________;加入二氧化锰时被氧化的物质是____________(填化学式)。
(3)已知Fe、Al、Mn的氢氧化物开始沉淀及沉淀完全时的pH如表所示,则加氨水沉淀时应控制溶液的pH范围为______________。此时得到的沉淀是____________、__________(填化学式)。
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀pH | 1.8 | 4.1 | 8.3 |
| 完全沉淀pH | 3.2 | 5.0 | 9.8 |
(4)电解硫酸锰溶液时,阴极的电极反应式为____________________。用酸性高锰酸钾溶液检验Mn2+,产生黑色沉淀,该反应的离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
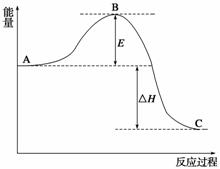
2SO2(g)+O2(g)2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。
请回答下列问题:
(1)图中A、C分别表示__________、__________,E的大小对该反应的反应热有无影响?__________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?____________,理由是_________________________________________________________;
(2)图中ΔH=__________kJ·mol-1;
(3)V2O5的催化循环机理可能为V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:________________________________________________________________________;
(4)已知常温下,1 mol固体硫燃烧生成二氧化硫气体时放出的热量是296 kJ,计算由S(s)生成3 mol SO3(g)的ΔH________(要求写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求回答下列问题:
(1)已知:4Al(s)+3O2(g)===2Al2O3(s)
ΔH=-2 834.9 kJ·mol-1①
Fe2O3(s)+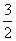 C(s)===
C(s)===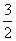 CO2(g)+2Fe(s)
CO2(g)+2Fe(s)
ΔH=+234.1 kJ·mol-1②
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1③
写出铝与氧化铁发生铝热反应的热化学方程式________________________________________________________________________。
(2)已知:
N2(g)+O2(g)===2NO(g) ΔH=+180.5 kJ·mol-1①
N2(g)+3H2(g)===2NH3(g)
ΔH=-92.4 kJ·mol-1②
2H2(g)+O2(g)===2H2O(g)
ΔH=-483.6 kJ·mol-1③
若有17 g氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是 ( )
A.水玻璃的主要成分是硅酸
B.相同温度下,Na2CO3的溶解度小于NaHCO3
C.H2O2中H元素的化合价是+2
D.醋酸的电离方程式:CH3COOH CH3COO- + H+
CH3COO- + H+
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学参阅了“84消毒液”说明中的配方,欲用NaClO固体配制480 mL含 NaClO 25%,密度为1.19 g/cm3的消毒液。下列说法正确的是 ( )
A.定容摇匀后,有少量溶液外流,则NaClO的物质的量浓度偏小
B.容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制
C.所配得的NaClO消毒液在空气中光照,久置后溶液中NaClO的物质的量浓度减小
D.需要称量的NaClO固体的质量为142.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中含有大量的氯化镁,从海水中提取镁的生产流程如下图所示:

回答下列问题:
(1)写出在海水中加入氧化钙生成氢氧化镁的化学方程式
;
(2)操作①主要是指 ;试剂①可选用 ;
(3)操作②是指 ;经操作③最终可得金属镁。
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为C10H14,属于苯的同系物,且苯环上的一氯代物只有2种的有机物有(不考虑立体异构,苯环上至少有3个氢)
A.5种 B.6种 C.7种 D.8种
查看答案和解析>>
科目:高中化学 来源: 题型:
某pH=1的工业废液,只可能含有以下离子中的若干种:H+、Mg2+、Ba2+、Cl-、CO 、SO
、SO ,现取两份100 mL溶液进行如下实验:
,现取两份100 mL溶液进行如下实验:
实验1:向第一份溶液中加入足量AgNO3溶液,干燥得沉淀3.50 g。
实验2:向第二份溶液中加入足量BaCl2溶液后,干燥得沉淀2.33 g,经足量盐酸洗涤、干燥后,沉淀质量不变。
根据上述实验,以下推测正确的是( )
①一定存在Mg2+ ②可能存在CO ③一定存在Cl- ④可能存在Ba2+ ⑤可能存在Mg2+
③一定存在Cl- ④可能存在Ba2+ ⑤可能存在Mg2+
A.①③ B.②③
C.③⑤ D.④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com