
| A. | S.O.K | B. | Na.C.O | C. | H.O.S | D. | H.N.O |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物是离子化合物,属于离子化合物;只含共价键的化合物是共价化合物,属于分子晶体,据此分析解答.
解答 解:A、K是活泼金属元素,S、O是非金属元素,这三种元素相互化合只能形成离子化合物(如硫酸钾),不能形成共价化合物,故A错误;
B、Na是活泼金属元素,C、O是非金属元素,这三种元素相互化合只能形成离子化合物(如碳酸钠),不能形成共价化合物,故B错误;
C、H、S、O是非金属元素,这三种元素相互化合只能形成共价化合物(如H2SO4),不能形成离子化合物,故C错误;
D、H、N、O是非金属元素,各元素相互化合可以共价化合物(如硝酸),属于分子晶体,也可以形离子化合物(如硝酸铵),属于离子晶体,故D正确;
故选:D.
点评 本题考查了元素与化学键的关系,难度不大,注意:金属元素和非金属元素形成的化合物不一定是离子化合物,如氯化铝是共价化合物不是离子化合物.


科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率关系是:3υ(NH3)═2υ(H2O) | |
| B. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大 | |
| D. | 达到化学平衡时,5υ正(O2)=4υ逆(NO) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属的熔点和沸点都很高 | |
| B. | H2O、CCl4都是含有极性键的非极性分子 | |
| C. | HF、HCl、HBr、HI的酸性依次增强 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
| A. | 元素X的常见化合价是+1 | |
| B. | 元素X与氯形成化合物时,化学式可能是XCl | |
| C. | 元素Y是ⅢA族元素 | |
| D. | 若元素Y处于第三周期,它可与冷水剧烈反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸雨就是指pH<7的雨水 | |
| B. | 工业上大量燃烧含硫燃料和以含硫矿石为原料冶炼金属产生的SO2是产生硫酸型酸雨的主要原因 | |
| C. | 酸雨是因为雨水中含有CO2 | |
| D. | 酸雨没有危害,所以不必担心,也不必想办法治理 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
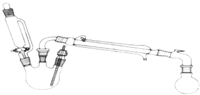 某研究性小组探究乙酸乙酯的反应机理,实验如下:已知:相关物理性质(常温常压)
某研究性小组探究乙酸乙酯的反应机理,实验如下:已知:相关物理性质(常温常压)| 密度g/mL | 熔点/℃ | 沸点/℃ | 水溶性 | |
| 乙醇 | 0.79 | -114 | 78 | 溶 |
| 乙酸 | 1.049 | 16.2 | 117 | 溶 |
| 乙酸乙酯 | 0.902 | -84 | 76.5 | 不溶 |
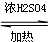 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
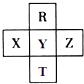 元素R、T、X、Y、Z在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸,生成HR.则下列判断正确的是( )
元素R、T、X、Y、Z在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸,生成HR.则下列判断正确的是( )| A. | 非金属性:Z<Y<X | |
| B. | R与Y的电子数相差8 | |
| C. | 气态氢化物稳定性:HR<HY<HT | |
| D. | 最高价氧化物的水化物的酸性:HTO4>HYO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com