
| ||
| 13.44L |
| 22.4L/mol |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| TiCl4 | Mg | MgCl2 | Ti | |
| �۵�/�� | -25.0 | 648.8 | 714 | 1667 |
| �е�/�� | 136.4 | 1090 | 1412 | 3287 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����ʺϵ�����������Ӧ2Fe3++2I-?2Fe2++I2��Ƴ���ͼ��ʾ��ԭ��أ������жϲ���ȷ���ǣ�������
�����ʺϵ�����������Ӧ2Fe3++2I-?2Fe2++I2��Ƴ���ͼ��ʾ��ԭ��أ������жϲ���ȷ���ǣ�������| A����Ӧ��ʼʱ������ʯī�缫��Fe3+����ԭ |
| B����Ӧ��ʼʱ������ʯī�缫�Ϸ���������Ӧ |
| C�������ƶ���Ϊ���ֵʱ����Ӧ�ﵽ��ѧƽ��״̬ |
| D�������ƶ���Ϊ����ڼ�������FeCl2���壬����ʯī�缫Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1����298Kʱ��1mol CH4����������ȫȼ�����ɶ�����̼��Һ̬ˮ���ų�����890.0kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ
��1����298Kʱ��1mol CH4����������ȫȼ�����ɶ�����̼��Һ̬ˮ���ų�����890.0kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
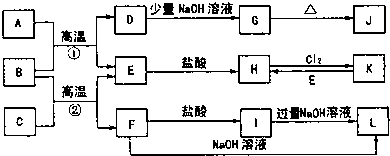
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��ͼ�ٱ�ʾһ�����淴Ӧ�ﵽƽ��״̬���ֿ���ʹ���˴��� |
| B��ͼ�������߱�ʾ��Ӧ2SO2��g��+O2��g��?2SO3��g����H��0�������淴Ӧ��ƽ�ⳣ��K���¶ȵı仯 |
| C���Է�ӦaA��g��+bB��g��?cC��g����˵��ͼ��x���ʾ����Ӧ��ѹǿ�����¸÷�Ӧ����������Ӧ������� |
| D��ͼ����a��b���߷ֱ��ʾ��ӦCH2=CH2��g����CH3CH3��g����H��0ʹ�ú�δʹ�ô���ʱ����Ӧ�����е������仯 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com