
 ����ԭ�ϣ���ҵ�������������Ҫ�������£�
����ԭ�ϣ���ҵ�������������Ҫ�������£�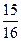 ����N2��ת����
����N2��ת����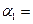 ��������ѹǿ�㶨���ﵽƽ��״̬ʱ��N=��ת����Ϊ
��������ѹǿ�㶨���ﵽƽ��״̬ʱ��N=��ת����Ϊ ����
����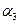
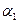 �����>������<����=������
�����>������<����=������ 4NO+6H2O 4NO+3O2+2H2O=4HNO3
4NO+6H2O 4NO+3O2+2H2O=4HNO3 0 mol��L-1��Na2CO3��Һ��Ӧ��ȫ��������NaNO2��NaNO3�����ʵ����ı�Ϊ4��1�����ڻ��������NO������������Ϊ����?����д��������̣�
0 mol��L-1��Na2CO3��Һ��Ӧ��ȫ��������NaNO2��NaNO3�����ʵ����ı�Ϊ4��1�����ڻ��������NO������������Ϊ����?����д��������̣� 
 �غ㣬��NaNO2��NaNO3�����ʵ����ֱ�Ϊ4a mol��a mol����4a+a=50mL��10-3mL��L-1��1��0 mol��L-1��2����ã�a=0��02 mol�����ǣ��Ƴ�NO��NO2�����ʵ�������Ϊ��0��03 mol��0��07 mol������NO��ռ���������Ϊ30����
�غ㣬��NaNO2��NaNO3�����ʵ����ֱ�Ϊ4a mol��a mol����4a+a=50mL��10-3mL��L-1��1��0 mol��L-1��2����ã�a=0��02 mol�����ǣ��Ƴ�NO��NO2�����ʵ�������Ϊ��0��03 mol��0��07 mol������NO��ռ���������Ϊ30����

 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д� ��Ȥ����¹�֪��ϵ�д�
��Ȥ����¹�֪��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
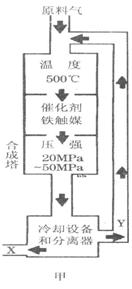
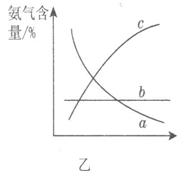
 ��ͼ��������ѡ������Ҫԭ���ǣ�ѡ����ĸ��ţ���ͬ��________��
��ͼ��������ѡ������Ҫԭ���ǣ�ѡ����ĸ��ţ���ͬ��________�� ijͬѧ�Ʋ����Һ�и�����Ũ�ȴ�С˳��������������ֹ�ϵ��
ijͬѧ�Ʋ����Һ�и�����Ũ�ȴ�С˳��������������ֹ�ϵ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

 ��1���ϳɰ���Ӧ��ӦN2��g��+3H2��g��
��1���ϳɰ���Ӧ��ӦN2��g��+3H2��g��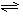 2NH3��g�������ں��¡���ѹ��������ƽ����ϵ��ͨ�������ƽ�� �ƶ�����������ҡ���������ʹ�ô��� ��Ӧ�Ħ�H���������С�����ı䡱����
2NH3��g�������ں��¡���ѹ��������ƽ����ϵ��ͨ�������ƽ�� �ƶ�����������ҡ���������ʹ�ô��� ��Ӧ�Ħ�H���������С�����ı䡱���� ��2����֪��N2H4��g��+O2��g��=N2��g��+2H2O��g������H=��543kJ��mol��1
��2����֪��N2H4��g��+O2��g��=N2��g��+2H2O��g������H=��543kJ��mol��1
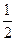 H2��g��+
H2��g��+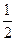 F2��g��=HF��g������H=��269kJ��mol��1
F2��g��=HF��g������H=��269kJ��mol��1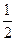 O2��g��=H2O��g������H=��242kJ��mol��1
O2��g��=H2O��g������H=��242kJ��mol��1 ��Ӧ N2H4��g��+2F2��g��=N2��g��+4HF��g����
��Ӧ N2H4��g��+2F2��g��=N2��g��+4HF��g����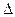 H="_____________" kJ��mol-1��
H="_____________" kJ��mol-1�� ��3����֪25��ʱKsp[Mg��OH��2]=1.8��10-11,KsP[Cu��OH��2]=2.2��10-20����25���£���Ũ�Ⱦ�Ϊ0.1 mol��L-1��MgCL2��CuCl2�����Һ����μ��백ˮ��������__________�������ѧʽ�������ɸó��������ӷ���ʽΪ______��
��3����֪25��ʱKsp[Mg��OH��2]=1.8��10-11,KsP[Cu��OH��2]=2.2��10-20����25���£���Ũ�Ⱦ�Ϊ0.1 mol��L-1��MgCL2��CuCl2�����Һ����μ��백ˮ��������__________�������ѧʽ�������ɸó��������ӷ���ʽΪ______�� ��4����25���£���a mol��L-1�İ�ˮ��0.01 mol��L-1������������ϣ���Ӧƽ��ʱ��Һ��c��NH4+��=c��Cl-��������Һ��_____________�ԣ���ᡱ������С������ú�a�Ĵ���ʽ��ʾ��ʱ��Һ��NH3��H2O�����ʵ���Ũ��__________ mol��L-1����˵������Һ���������ֱ����ӣ�
��4����25���£���a mol��L-1�İ�ˮ��0.01 mol��L-1������������ϣ���Ӧƽ��ʱ��Һ��c��NH4+��=c��Cl-��������Һ��_____________�ԣ���ᡱ������С������ú�a�Ĵ���ʽ��ʾ��ʱ��Һ��NH3��H2O�����ʵ���Ũ��__________ mol��L-1����˵������Һ���������ֱ����ӣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
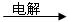 A + B + C
A + B + C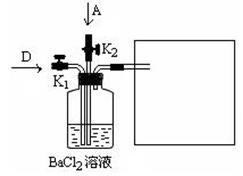
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 3NH3(g) ��H����92.2kJ/mol���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2����̼�ڸ�������ˮ������Ӧ�Ƶá��ҹ��ϳɰ���ҵĿǰ����������Ϊ������������ý���¶ȣ�400��500�棬ѹǿ��30��50MPa���ش��������⣺
3NH3(g) ��H����92.2kJ/mol���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2����̼�ڸ�������ˮ������Ӧ�Ƶá��ҹ��ϳɰ���ҵĿǰ����������Ϊ������������ý���¶ȣ�400��500�棬ѹǿ��30��50MPa���ش��������⣺ H2(g) + CO(g) ��H =" +131.3" kJ ����S =" +133.7" J/K
H2(g) + CO(g) ��H =" +131.3" kJ ����S =" +133.7" J/K 2NH3(g) ��K=0.5��
2NH3(g) ��K=0.5�� N2 (g)+ 3H2(g)��K= ������ֵ����
N2 (g)+ 3H2(g)��K= ������ֵ����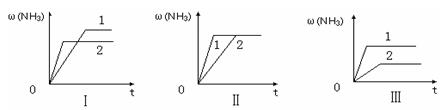
| A��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��P2��P1 |
| B��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��P1��P2 |
| C��ͼ������Dz�ͬ�¶ȶԷ�Ӧ��Ӱ�죬��T1��T2 |
| D��ͼ�������ͬ��ͬѹ�£��������ܣ�1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ά | B�������оƬ | C��ʯӢ�ӱ� | D��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A������ԭú���������ɼ���ȼú������SO2 | B�������Ƶ�ˮ��Һ�׳�ˮ������������ľ�ķ����� |
| C��ˮ���Ȳ�����ˮҲ�������κ��� | |
| D��ˮ�ࡢ�������ǹ�������Ʒ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
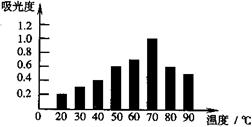
| A��20��ʱ�������к�ɫ�غ������ | |
| B�������Խ�����к�ɫ�غ���Խ�� | C����ɫ�ؿ����ڽϸ��¶��²��ȶ� |
| D���¶�Խ�ߣ���ȡҺ�к�ɫ�غ���Խ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Ӳˮ������ | B����ⱥ��ʳ��ˮ����NaOH |
| C��������������ˮ | D����ˮ����ȡ����Mg |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com