
【题目】苯甲酸广泛用于医药、食品、染料、化工等领域。以下是实验室制备苯甲酸的一种方法。反应原理:
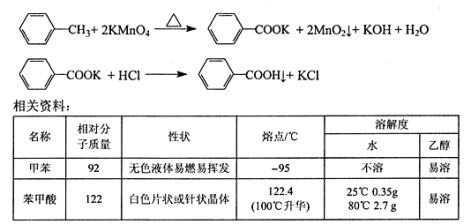

实验步骤:
①下图组装反应装置(冷凝水、夹持及加热装置未画出),并在三颈烧瓶中依次加入120mL水、稍过量高锰酸钾和3.0mL甲苯(密度为0.866g/ mL)。
②将三颈烧瓶中的混合液体搅拌、加热至沸腾,直到甲苯完全反应。
③趁热过滤反应混合物。若滤液呈紫色,则需加入适量的亚硫酸氢钠溶液至紫色褪去后再过滤,用热水洗涤滤渣,洗涤液合并至滤液中。
④用冰水冷却滤液,然后用浓盐酸酸化,过滤,用少量冷水洗涤滤渣,得到苯甲酸粗产品,经重结晶得到精制的苯甲酸。
回答下列问题:
(1)仪器 a名称为 。
(2)判断甲苯己完全反应的现象是 、回流液不再出现油珠。
(3)实验步骤④中,用少量冷水而不用热水洗涤滤渣的目的是 ;苯甲酸粗产品除了可用重结晶法精制外,还可用 法。
(4)精制的苯甲酸纯度测定:称取1.220g样品,用稀乙醇溶解并配成100 mL溶液,分别取25.00mL溶液,用0.1000 mo1·L-1NaOH标准溶液滴定,三次滴定消耗NaOH溶液的体积分别为V1=22.48mL.V2=22.52 mL.V3= 23.80mL。
①配制溶液时用稀乙醇而不用蒸馏水作溶剂的原因是 。
②若用酚酞作指示剂,确定滴定终点的现象是 。
③产品的纯度为 。
【答案】(1)(蛇形)冷凝管
(2)三颈烧瓶中混合液不再分层(或甲苯层消失)
(3)减少苯甲酸因溶解造成损失,升华
(4)①常温下苯甲酸微溶于水而易溶于乙醇②滴加最后一滴氢氧化钠标准溶液后,溶液由无色变为浅红色,且30秒不褪色③90%(3分)
【解析】
试题分析:(1)根据仪器的特征,仪器 a名称为(蛇形)冷凝管。
(2)因为甲苯不溶于水,但苯甲酸能溶于水,所以甲苯完全反应的现象为三颈烧瓶中混合液不再分层(或甲苯层消失)。
(3)因为苯甲酸能溶于水,所以用少量冷水可以减少苯甲酸因溶解造成损失,因为苯甲酸能升华,所以可以采用升华的方法分离。
(4)①常温下苯甲酸微溶于水而易溶于乙醇,所以配制溶液时用稀乙醇不用蒸馏水。②用酚酞做指示剂,滴定终点的现象为滴加最后一滴氢氧化钠标准溶液后,溶液由无色变为浅红色,且30秒不褪色。③V3数据与其他的数据差距大,所以舍去,求体积平均值为22.50毫升,所以纯度=4×22.50×0.1×122/(25×1.22)=90.00%。


科目:高中化学 来源: 题型:
【题目】下列叙述中,错误的是( )
A.沙里淘金是利用金与沙的密度相差较大而将沙淘走,使金留下
B.化学上所指的杂质,有的本来无害且很有价值,即使有害无价值的也应设法变废为宝
C.检验某溶液时,将检测试剂一次加入全部溶液里
D.蒸发时加热到蒸发皿出现较多固体时即可
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电池的研究一直是化学工作者研究的热点之一.
Ⅰ.美国科学家S鲁宾成功开发锌汞纽扣式电池,以锌和氧化汞为电极材料,氢氧化钾溶液为电解液的原电池,有效地解决电池使用寿命短,易发生漏液等问题.电池总反应为:Zn+HgO═ZnO+Hg。
(1)该电池的正极反应式为 。
(2)含汞电池生产企业的污水中会含有一定量的+2价的汞离子,通常采用处理成本较低的硫化物沉淀法,即向污水中投入一定量的硫化钠,反应的离子方程式为 。
(3)该方法的缺点是产物的颗粒比较小,大部分悬浮于污水中,通常采用投入一定量的明矾晶体进行后续处理,请解释其原因 。
Ⅱ.锂离子电池由于轻便、比能量大等优点,成为当今社会最为常见的电池.其中的重要材料磷酸亚铁锂(LiFePO4)通常按照下列流程进行生产:

请回答下列问题:
(4)生产过程中“混合搅拌”的目的是 。气体X的化学式为 。
(5)请写出一定条件下由LiH2PO4生成LiFePO4的化学方程式 ,当生成1mol磷酸亚铁锂时,转移的电子数目为 。
(6)生成LiFePO4的过程可能产生一种杂质对电池有致命的影响,则该杂质可能为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到实验目的的是( )
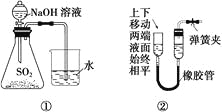
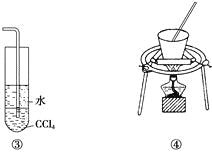
A. 装置①可用于证明SO2与NaOH溶液发生了反应
B. 装置②可证明装置的气密性良好
C. 装置③可用于吸收NH3或HCl气体,并防止倒吸
D. 装置④可用于实验室从食盐水中提取氯化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴(Co)及其化合物在工业上有广泛应用。为从某工业废料中回收钴,某学生设计流程如下(废料中含有Al、Li、Co2O3和Fe2O3等物质)。

已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表:
Fe3+ | Co2+ | Co3+ | Al3+ | |
pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
请回答:
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式是 。
(2)写出步骤Ⅱ中Co2O3与盐酸反应的离子方程式 。有同学认为Ⅱ中将盐酸换成硫酸和H2O2溶液更好,请结合离子方程式说明理由 。
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过__________。废渣中的成分有_________________。
(4)在空气中加热CoC2O4固体,经测定,210~290℃的过程中只产生CO2和一种二元化合物,该化合物中钴元素的质量分数为73.44%。此过程发生反应的化学方程式是_______________。
(5)某锂离子电池的总反应为C6+LiCoO2 ![]() LixC6+Li1-xCoO2,LixC6中Li的化合价为______价,该锂离子电池充电时阳极的电极反应式为 。
LixC6+Li1-xCoO2,LixC6中Li的化合价为______价,该锂离子电池充电时阳极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据泡利的原子轨道能级图和“能级交错”现象,原子轨道的能量高低顺序是:
ns<(n-3)g<(n-2)f<(n-1)d<np(n为能层序数,g能级中有9个轨道)。则未来的第八周期应包括的元素的种类是
A. 128 B. 64 C. 50 D. 32
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂质(括号中物质为杂质)所用试剂或方法不正确的是( )
A. CO2(CO):O2
B. MgO(Al203): NaOH溶液
C. NaHCO3溶液(Na2CO3):过量的C02
D. C02( HCl): 饱和NaHC03溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中的杂质,所用试剂和方法不正确的是( )
物质 | 杂质 | 除杂所用试剂和方法 | |
A | KCl溶液 | I2 | 酒精,萃取 |
B | KNO3 | K2SO4 | Ba(NO3)2溶液,过滤 |
C | Cu | CuO | 盐酸,过滤 |
D | CaCO3 | CaO | H2O,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据表,下列说法正确的是()

A.25°C时,pH=3的醋酸和pH=11的氨水等体积混合后,混合液中水的电离是被促进的
B.Na2SO3溶液中滴加足量醋酸,反应的离子方程式为:SO3 +2CH3COOH=SO2↑+H2O+2CH3COO-
C. NaHSO3溶液呈酸性,是因为Kw/Ka1>Ka2
D.0.1mol/L的CH3COOH溶液与等浓度等体积的CH3COONa 混合后,溶液中的微粒存在以下关系: c (H+) +c (CH3COOH) =c (CH3COO-) +2c (OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com