
| m |
| M |
| 溶质质量 |
| 溶液质量 |
| m |
| M |
| m |
| M |
| 2mNA |
| M |
| 2mNA |
| M |
| 1000dw |
| 24 |
| 1000dw |
| 24 |
| 1000dw |
| 12 |
| 1000dw |
| 12 |
| amL |
| 1000mL |
| adw |
| 12 |
| adw |
| 12 |
| 溶质质量 |
| 溶液质量 |
| ||
|
| 17V |
| 17V+22400 |
| 17V |
| 17V+22400 |
| 17V |
| 17V+22400 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、植物油能使溴的四氯化碳溶液褪色 |
| B、葡萄糖能发生氧化反应和水解反应 |
| C、蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |
| D、油脂的水解又叫皂化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子数 | B、密度 |
| C、质量 | D、质子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氟利昂化学性质稳定、有毒 |
| B、氟利昂会产生温室效应 |
| C、氟利昂会破坏臭氧层 |
| D、氟利昂会形成酸雨 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
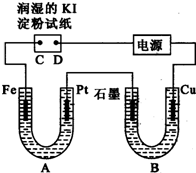 电解装置如图所示.图中B装置盛1L 3mol?L-1 K2SO4溶液,A装置中盛1L 3mol?L-1 AgNO3溶液.通电一段时间后,润湿的淀粉KI试纸的C端变蓝色.试回答:
电解装置如图所示.图中B装置盛1L 3mol?L-1 K2SO4溶液,A装置中盛1L 3mol?L-1 AgNO3溶液.通电一段时间后,润湿的淀粉KI试纸的C端变蓝色.试回答:| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g?cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com