
| A. | 6.7% | B. | 8.7% | C. | 9% | D. | 12.5% |
分析 CH3OH、CH3COOH和丙三醇(C3H8O3)组成的混合液体,各组分中C、O原子数目之比均为1:1,则混合物中二者质量之比为12:16=3:4,进而计算O元素质量分数,混合物中H元素质量=1-w(C)-w(O).
解答 解:CH3OH、CH3COOH和丙三醇(C3H8O3)组成的混合液体,各组分中C、O原子数目之比均为1:1,则混合物中二者质量之比为12:16=3:4,故混合物中O元素质量分数为39%×$\frac{4}{3}$=52%,则混合物中H元素质量=1-39%-52%=9%,
故选:C.
点评 考查混合物中元素的质量分数的计算,难度中等,关键是利用混合物中各成分的化学式得出C、O的固定组成.


 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
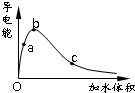 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示:
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
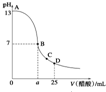 25℃时,在25mL 0.1mol•L-1的NaOH溶液中,逐滴加入0.2mol•L -1的CH3COOH溶液,溶液的pH与醋酸体积关系如图所示,下列分析不正确的是( )
25℃时,在25mL 0.1mol•L-1的NaOH溶液中,逐滴加入0.2mol•L -1的CH3COOH溶液,溶液的pH与醋酸体积关系如图所示,下列分析不正确的是( )| A. | B点的横坐标a>12.5 | |
| B. | C点时溶液中有:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | D点时溶液中有:c(CH3COO-)+c(CH3COOH)=2c(Na+) | |
| D. | 曲线上A、B间的任意一点,溶液中都有:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
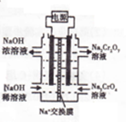
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;反应类型:加聚反应.
;反应类型:加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl | B. | CO2 | C. | NH3 | D. | CO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28 g C2H4所含共用电子对数目为4NA | |
| B. | 1 L 0.1 mol•L-1乙酸溶液中H+数为0.1NA | |
| C. | 1 mol甲烷分子所含质子数为10NA | |
| D. | 标准状况下,22.4 L乙醇的分子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com