
下列反应原理不符合工业冶炼金属实际情况的是
A.2CuO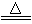 2Cu+O2↑
2Cu+O2↑
B.2NaCl(熔融) 2Na+Cl2↑
2Na+Cl2↑
C.2MgCl2(熔融) 2Mg+Cl2↑
2Mg+Cl2↑
D. Fe2O3+3CO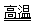 2Fe+3CO2
2Fe+3CO2
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
医学界通过用14C标记的C60发现一种羧酸衍生物,在特定条件下,它可以通过断裂DNA抑制艾滋病病毒的繁殖。下列有关叙述中,正确的是
A.14C与12C的化学性质完全不同
B.14C与14N含有的中子数相同
C.14C60和12C60是碳元素的同素异形体
D.14C与12C、13C互为同位素
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期第一次阶段考试化学试卷(解析版) 题型:选择题
下列实验过程中,始终无明显现象的是( )
A.CO2通入饱和Na2CO3溶液中
B.CO2通入CaCl2溶液中
C.NH3通入AlCl3溶液中
D.SO2通入已酸化的Ba(NO3)2溶液中
查看答案和解析>>
科目:高中化学 来源:2015届福建省、安溪一中高三上学期期中联考化学试卷(解析版) 题型:选择题
下列各组离子在给定条件下,能大量共存的是
A.含有NO3—的水溶液中:NH4+、Fe2+、SO 42— 、H+
B.含有CO32—的澄清透明溶液中:K+、NO3—、Cl—、Na+
C.在pH=2的溶液中:ClO—、SO32—、Na+ 、K+
D.能与铝粉反应生成氢气的溶液中:Na+、Al3+、CH3COO— 、I—
查看答案和解析>>
科目:高中化学 来源:2015届福建省、安溪一中高三上学期期中联考化学试卷(解析版) 题型:选择题
下列条件下,两瓶气体所含原子数、分子数一定相等的是
A.同温度、同体积的N2和CO B.同密度、同体积的H2和N2
C.同温度、同压强的C2H4和C3H6 D.同质量、不同密度的N2O和CO2
查看答案和解析>>
科目:高中化学 来源:2015届福建省、安溪第一中学高三9月摸底考试化学试卷(解析版) 题型:填空题
(11分)元素A、B、C、D均为短周期元素,请根据表中信息回答下列问题。
元素 | A | B | C | D |
性质 结构 信息 | 单质制成的高压灯,发出的黄光透雾力强、射程远。 | 工业上通过分离液态空气获得其单质。原子的最外层未达到稳定结构。 | 单质常温、常压下是气体,原子的M层有一个未成对的p电子。 | +3价阳离子的核外电子排布与氖原子相同。 |
(1)上表中与A属于同一周期的元素是 (填元素符号),D离子的核外电子排布式为 ;
(2)A和B形成的化合物晶体类型为 ;C单质与氢氧化钠溶液反应的离子方程式为 ;
(3)对元素B的相关描述正确的是 。
a.B元素的最高正价可能为+6 b.常温、常压下B单质难溶于水
c.B单质分子中含有18个电子 d.在一定条件下B单质能与镁条反应
查看答案和解析>>
科目:高中化学 来源:2015届福建省、安溪第一中学高三9月摸底考试化学试卷(解析版) 题型:选择题
下列溶液中各微粒的浓度关系不正确的是
A.0.1 mol/L的HCOOH溶液中:c(HCOO—)+c(OH—)=c(H+)
B.1 L 0.1 mol/L的CuSO4·(NH4)2SO4·6H2O的溶液中: c(SO42—)>c(NH4+)>c(Cu2+)>c(H+)>c (OH—)
C.0.1 mol/L 的NaHCO3溶液中: c(Na+)+c(H+)=c(HCO3—)+2c(CO32—)+c(OH—)
D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:
c(Na+)>c(HX)>c(X—)>c(H+)>c(OH—)
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中质量检测化学试卷(解析版) 题型:实验题
某中学研究性学习小组为探究碳酸钠和碳酸氢钠两种物质的性质、制法和用途,进行了如下实验:
实验一、如图Ⅰ~Ⅳ所示。
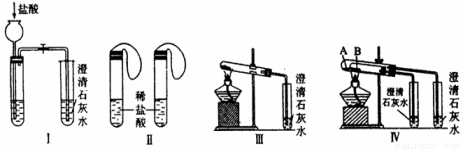
(1)若用实验Ⅳ来验证碳酸钠和碳酸氢钠的热稳定性,则试管B中装入的固体最好是 。
(2)若用实验来鉴别碳酸钠和碳酸氢钠两种固体,能达到实验目的的是(填装置序号) 。其中能够说明泡沫灭火器中选择碳酸氢钠与酸反应制CO2而不选择碳酸钠的实验是 。
(3)若测定Na2CO3固体中混有的少量NaHCO3的质量分数,采用实验Ⅲ能否达到实验目的? (填能或不能)。若能,请说明其计算所需的数据 ;若不能,请简要说明理由 。
实验二、将碳酸氢钠溶液与澄清石灰水混合并充分反应。
当石灰水过量时,反应的离子方程式为 。
实验三、检验“侯氏制碱法”制得的纯碱中是否混有食盐和小苏打。
(1)检验纯碱中是否混有食盐的试剂是 ;
(2)证明纯碱中混有小苏打的实验方法是 。
查看答案和解析>>
科目:高中化学 来源:2015届福建省四地六校高三上学期第一次月考化学试卷(解析版) 题型:填空题
(16分)亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
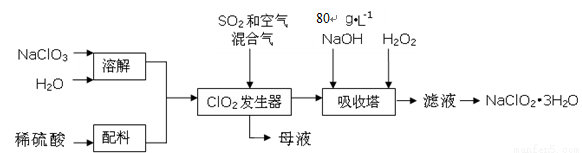
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2?3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③80 g·L-1 NaOH溶液是指80 g NaOH固体溶于水所得溶液的体积为1L。
(1)80 g·L-1 NaOH溶液的物质的量浓度为 ;
(2)发生器中鼓入空气的作用可能是 (选填序号);
a.将SO2氧化成SO3,增强酸性 b.将NaClO3氧化成ClO2 c.稀释ClO2以防止爆炸
(3)从“母液”中可回收的主要物质是 ;
(4)吸收塔内的反应的化学方程式为 ;
吸收塔的温度不能超过20℃,其目的是 ;
(5)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是 ;
(6)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是 (选填序号);
a.Na2S b.Na2O2 c.FeCl2
(7) 从吸收塔出来的溶液中得到NaClO2?3H2O粗晶体的实验操作依次是 (选填序号)。
a.蒸发浓缩 b.蒸馏 c.过滤 d.灼烧 e.冷却结晶
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com