
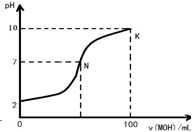
 常温下,向l00mL 0.01mol?L-1 盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )
常温下,向l00mL 0.01mol?L-1 盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )| A、MOH是弱碱 | ||
| B、N点c(Cl-)=c(M+) | ||
| C、K点对应的溶液c(MOH)+c(OH-)-c(H+)=0.001 mol?L-1 | ||
D、随着MOH溶液的滴加,比值
|
| c(M+)?c(OH-) |
| c(MOH) |


科目:高中化学 来源: 题型:
| A、电荷守恒:c(Na+)+c(H+)=c(A-)+c(Cl-)+c(OH-) |
| B、物料守恒:c(HA)+c(A-)=0.1mol/L |
| C、质子守恒:c(HA)+c(H+)=c(A-)+c(OH-) |
| D、物料守恒:c(Na+)=c(A-)+c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、地震灾区用漂白粉消毒,是利用漂白粉溶液的碱性 |
| B、鱼、肉、鸡蛋等富含蛋白质的食品被称为碱性食品,长期缺乏可使尿液偏酸性 |
| C、生铁在潮湿的空气中易生锈,其负极反应式为2H2O+O2+4e-═4OH- |
| D、实验室储存的镁条着火时,不可以用泡沫灭火器灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| Cl2 |
| ① |
| 480-530℃ |
| ② |
| 聚合 |
| 2200℃~2300℃ |
| HgCl2 |
| 140℃~200℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁元素属于过渡元素,其原子序数为26 |
| B、单质铁与浓硫酸在常温下不反应 |
| C、铁单质只具有还原性,其阳离子只具有氧化性 |
| D、与相同浓度的盐酸反应生成氢气的速率,纯铁比生铁的快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从铝土矿中分离出氧化铝的过程中不涉及氧化还原反应 |
| B、纯净的二氧化硅有优良的光学性能,可制成光电池和光导纤维 |
| C、海水中含有大量的钠元素,只需经过物理变化就可以得到钠单质 |
| D、Na+、Mg2+、Al3+得电子能力很弱,故常用电解熔融氧化物的方法来制备其单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强碱性溶液中:K+、Mg2+、Cl-、SO42- |
| B、水电离出来的c(H+)=10-13mol/L的溶液 K+、HCO3-、Br-、Ba2+ |
| C、所含溶质为Na2SO4的溶液 K+、CO32-、NO3-、Al3+ |
| D、室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com