
【题目】列举一个可以说明氯和硫的非金属性强弱的事实。______________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】除去物质中所含少量杂质(括号内为杂质),所选用试剂和分离方法能达到实验目的是
混合物 | 试剂 | 分离方法 | |
A | 苯(苯酚) | 溴水 | 过滤 |
B | 乙烷(乙烯) | 酸性高锰酸钾 | 洗气 |
C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
D | 溴苯(液溴) | NaOH溶液 | 分液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色透明溶液中,能大量共存的离子组是
A. K+、MnO4―、SO42―B. Al3+、Cl―、SO42―
C. Na+、CH3COO―、H+D. OH―、Na+、Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝。电解铝时阳极产生的CO2,可通过二氧化碳甲烷化再利用。
请回答:
⑴已知:2Al2O3(s)=4Al(g)+3O2(g) △H1=3351 kJ·mol-1
2C(s)+O2(g)=2CO(g) △H2=-221 kJ·mol-1
2Al(g) + N2(g)=2AlN(s) △H3=-318 kJ·mol-1
碳热还原Al2O3合成AlN的总热化学方程式是_____,该反应自发进行的条件____________。
(2)在常压,Ru/TiO2催化下,CO2和H2混合气体(体积比1:4,总物质的量a mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)。
反应I CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H1
CH4(g)+2H2O(g) △H1
反应II CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2

①下列说法不正确的是_____
A. △H1小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1:3,可提高CO2平衡转化率
②350℃时,反应I在t1时刻达到平衡,平衡时容器体积为VL,该温度下反应I的平衡常数为________(用a、V表示)。
③350℃下CH4物质的量随时间的变化曲线如图3所示。画出400℃下0~t1时刻CH4物质的量随时间的变化曲线。________

据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别称取2.39g(NH4)2SO4和NH4Cl固体混合物两份。
(1)将其中一份配成溶液,逐滴加入一定浓度的Ba(OH)2溶液,产生的沉淀质量与加入Ba(OH)2溶液体积的关系如图。混合物中n[(NH4)2SO4]:n(NH4Cl)为___________。

(2)另一份固体混合物中NH4+与Ba(OH)2溶液(浓度同上)恰好完全反应时,溶液中c(Cl-)=_____(溶液体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1molL1稀盐酸。下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是()
A. 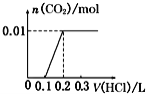 B.
B. 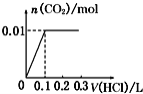 C.
C. 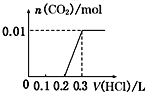 D.
D. 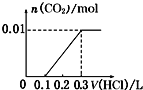
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列有关叙述正确的是
A. CO2的摩尔质量是44
B. NA个SO2分子的质量是64g
C. 1L1mol·L-1Na2SO4溶液中Na+数为NA
D. 9gH2O中氧原子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com