
【题目】工业上用某矿渣(含有Cu2O、Al2O3,Fe2O3、SiO2)制取铜的操作流程如下:
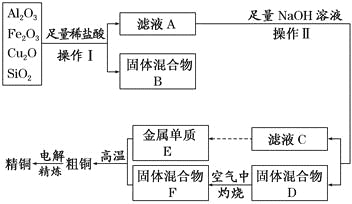
已知:Cu2O+2H+= Cu+Cu2++H2O
(1)实验操作Ⅰ的名称为 ;在空气中灼烧固体混合物D时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有 (填仪器名称)。
(2)滤液A中铁元素的存在形式为 (填离子符号),生成该离子的离子方程式为 ,检验滤液A中存在该离子的试剂为 (填试剂名称)。
(3)金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为 。
(4)常温下,等pH的NaAlO2和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍,则两种溶液的pH= 。
(5)利用电解法进行粗铜精炼时,下列叙述正确的是 (填代号)。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.精铜作阴极,电解后电解液中Cu2+浓度减小
d.粗铜精炼时通过的电量与阴极析出铜的量无确定关系
(6)从浓硫酸、浓硝酸、蒸馏水中选用合适的试剂,测定粗铜样品中金属铜的质量分数,涉及的主要步骤为:称取一定质量的样品→ →过滤、洗涤、干燥→称量剩余固体铜的质量。(填缺少的操作步骤,说出主要操作方法,不必描述操作过程的细节)
【答案】(1)过滤;坩埚;
(2)Fe2+;Cu+2Fe3+===Cu2++2Fe2+;硫氰化钾溶液和新制氯水或铁氰化钾溶液;
(3)2Al+Fe2O3![]() 2Fe+Al2O3;(4)11;
2Fe+Al2O3;(4)11;
(5)b c;(6)将浓硫酸用蒸馏水稀释,使样品与足量稀硫酸充分反应。
【解析】试题分析:(1)操作I得到液体和固体,因此操作步骤为过滤;灼烧固体需要在坩埚中进行,因此缺少的是坩埚;
(2)Cu2O在酸性条件生成Cu,Fe2O3+6H+=2Fe3++3H2O,Cu+2Fe3+=Cu2++2Fe2+,因此铁元素以Fe2+形式存在;检验Fe2+:先加KSCN溶液,观察溶液颜色,然后再加氯水,如果溶液变为红色,说明含有Fe2+,也可以用K3Fe(CN)6,如果产生蓝色沉淀,说明有Fe2+;
(3)焊接钢轨,采用铝热反应,即2Al+Fe2O3![]() 2Fe+Al2O3;
2Fe+Al2O3;
(4)设pH=x,NaOH溶液中水电离出c(OH-)=c(H+)=10-x,则NaAlO2中水电离的c(OH-)=10(8-x),NaAlO2的pH=10-14/10(8-x)=10(x-22),两者pH相等,则有x=22-x,解得x=11;
(5)a、电解过程一部分能量转化成热能,故错误;b、精炼铜时,粗铜作阳极,发生氧化反应,纯铜作阴极,化合价降低,发生还原反应,故正确;c、粗铜中含有锌、铁等杂质,Zn-2e-=Zn2+,阴极上:Cu2++2e-=Cu,溶液Cu2+略有降低,故正确;d、阴极:Cu2++2e-=Cu,能够得到通过的电量和析出铜的量的关系,故错误;(6) 将浓硫酸用蒸馏水稀释,使样品与足量稀硫酸充分反应。


科目:高中化学 来源: 题型:
【题目】用下列装置进行相应实验,能达到实验目的的是

图1 图2 图3 图4
A. 图1所示装置制取并收集氨气
B. 图2所示装置用于制备并收集NO气体
C. 图3所示装置用于除去碳酸氢钠固体中的少量碳酸钠
D. 图4所示装置用于Na2CO3和稀H2SO4反应制取少量的CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有如下的可逆反应:X(g)+2Y(g)![]() 2Z(g) 现将X和Y以1︰2的体积比混合在密闭容器中,加压到3×107Pa,达到平衡后,已知平衡状态时反应物的总物质的量和生成物的总物质的量相等时,对应图中坐标上的温度是( )
2Z(g) 现将X和Y以1︰2的体积比混合在密闭容器中,加压到3×107Pa,达到平衡后,已知平衡状态时反应物的总物质的量和生成物的总物质的量相等时,对应图中坐标上的温度是( )

A. 100℃ B. 200℃ C. 300℃ D. 不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
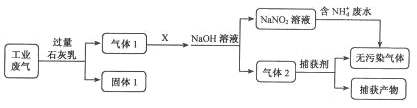
己知:NO+NO2+NaOH=NaNO2+H2O
2NO2+2NaOH=NaNO3+NaNO2+H2O
请回答下列问题:
(1)固体1中主要含有_________________________ (用化学式表示);
(2)X可以是________(填物质名称),且该物质需要________(填“少量”或“过量”);
(3)捕获剂所捕获的气体主要是________(用化学式表示);
(4)处理含NH4+废水时,发生反应的离子方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的氨基甲酸置于恒容的密闭真空容器中(固体体积忽略不计),使其达到化学平衡:H2NCOONH4(s)![]() 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
下列有关叙述正确的是
A. 在低温下该反应能自发进行
B. 15℃时,该反应的化学平衡常数约为2.0
C. 当混合气体平均相对分子质量不变时,该反应达到化学反应限度
D. 恒温条件下,向原平衡体系中再充入2molNH3和1molCO2,达平衡后CO2浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A由碳、氢、氧三种元素组成。现取3g A与4.48L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重3.6g,碱石灰增重4.4g。回答下列问题:
(1)3gA中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
(3)写出有机物A可能的结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于烷烃的说法中,正确的是( )
A.通式为CnH2n
B.可以使酸性高锰酸钾溶液褪色
C.在光照下可与氯气发生加成反应
D.随分子中碳原子数的增加,烷烃的熔沸点升高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com