

分析 A是铁锈的主要成分是氧化铁,与一氧化碳反应生成单质铁和二氧化碳,铁与氯气反应生成氯化铁,所以固体C为氯化铁,氯化铁与二氧化硫与水反应生成硫酸亚铁,硫酸亚铁溶液中加入氯化钡生成白色沉淀硫酸钡,则E是硫酸钡,由此分析解答.
解答 解:A是铁锈的主要成分是氧化铁,与一氧化碳反应生成单质铁和二氧化碳,铁与氯气反应生成氯化铁,所以固体C为氯化铁,氯化铁与二氧化硫与水反应生成硫酸亚铁,硫酸亚铁溶液中加入氯化钡生成白色沉淀硫酸钡,则E是硫酸钡,
(1)白色沉淀硫酸钡的化学式BaSO4,故答案为:BaSO4;
(2)一氧化碳还原氧化铁的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)氯化铁与二氧化硫与水反应生成硫酸亚铁,反应的离子方程式为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
点评 本题考查铁的单质及化合的相关性质,学生要会分析流程图解相关知识,综合性强有一定的难度.


科目:高中化学 来源: 题型:解答题
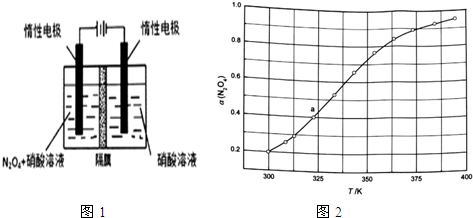
| t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| c(N2O5)/mol/L | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
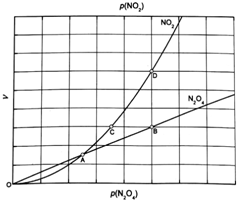
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
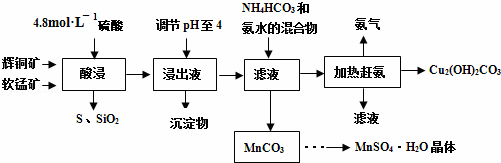
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
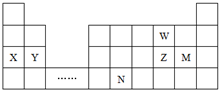
| A. | 原子半径:Y>Z>W | |
| B. | 单质的还原性:X>Y | |
| C. | 溴与元素M同主族,最高价氧化物的水化物的酸性比M的强 | |
| D. | 元素N位于金属与非金属的分界线附近,可以推断N元素的单质可作半导体材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(HCl)>c(CH3COOH) | |
| B. | c(Cl-)=c(CH3COO-) | |
| C. | 等体积的盐酸和醋酸溶液分别与足量的Zn完全反应,盐酸产生的H2多 | |
| D. | 用同浓度的NaOH溶液分别与等体积的盐酸和醋酸溶液恰好反应完全,盐酸消耗的NaOH溶液体积多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室里易燃试剂与强氧化性试剂应分开放置并远离火源 | |
| B. | 在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即读出并记录溶液的起始温度,充分反应后再读出并记录反应体系的最高温度 | |
| C. | 滴定实验中所用到的滴定管和移液管,在使用前均需干燥或用相应的溶液润洗,容量瓶、锥形瓶则不应润洗 | |
| D. | 将含有少量氯化钾的硝酸钾放入烧杯中,加水溶解并加热、搅拌,当溶液表面出现一层晶膜时停止加热,冷却结晶,过滤即可得到大量硝酸钾晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
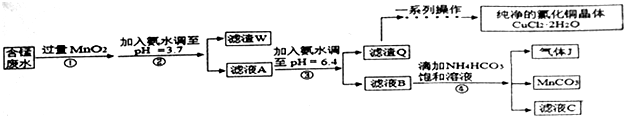
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
| 开始沉淀的pH | 7.5 | 3.2 | 5.2 | 8.8 |
| 完全沉淀的pH | 9.7 | 3.7 | 6.4 | 10.4 |
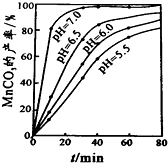
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
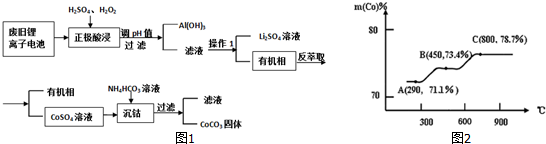
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com