
| A、①②③ | B、①③⑤ |
| C、②④⑤ | D、④⑤⑥ |


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:高中化学 来源: 题型:
 如表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
如表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )| a | b | c | |
| A | Al | AlCl3 | Al(OH)3 |
| B | Al2O3 | AlO2- | Al(OH)3 |
| C | Na | Na2O | NaOH |
| D | Si | SiO2 | H2SiO3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol氢气所含的原子数目为NA |
| B、17g氨气所含有氢原子数为3 NA |
| C、11.2L氮气所含的原子数目为NA |
| D、同温同压下,相同体积的任何气体单质所含有的原子数相同,均为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2NO+O2=2NO2 |
| B、N2+O2=2NO |
| C、N2+3H2=2NH3 |
| D、3NO2+H2O=2HNO3+NO |
查看答案和解析>>
科目:高中化学 来源: 题型:
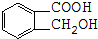 .试回答:
.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
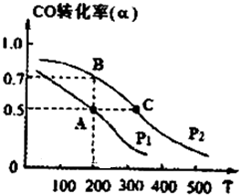 工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:| 1 |
| 2 |
| C(H2) |
| C(CH3OH) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com