
2- 4 |
| m |
| M |
| n |
| V |
| n |
| V |
| 2.33g |
| 233g/mol |
| 0.01mol |
| 0.1L |
| 4.275g |
| 171g/mol |
| 0.04mol |
| 0.1L |
| 0.02mol |
| 0.1L |


科目:高中化学 来源: 题型:
| A、C的生成速率与C分解的速率相等 |
| B、单位时间生成nmolA,同时生成3nmolB |
| C、单位时间生成nmolA,同时生成2nmolC |
| D、单位时间生成B的速率与生成C的速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na、Fe分别与不足量的稀硫酸反应所得溶液均呈中性 |
| B、7.8gNa2O2与CO2完全反应,转移0.2mol电子 |
| C、能通过化合反应制得FeCl3和Fe(OH)3 |
| D、NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
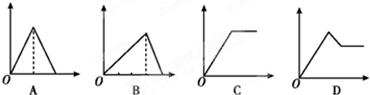
查看答案和解析>>
科目:高中化学 来源: 题型:
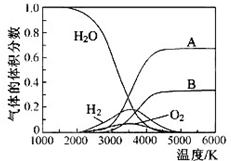 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.查看答案和解析>>
科目:高中化学 来源: 题型:
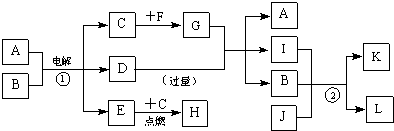
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com