
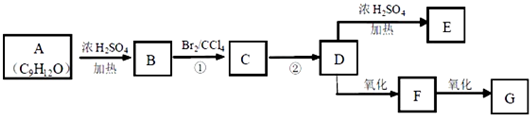
| 9×2+2-12 |
| 2 |
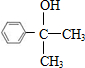 ,则B为
,则B为 ,C为
,C为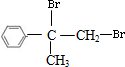 ,红外光谱图显示D中有两个相同的官能团,且D能连续氧化,说明D中含有醇羟基,则C生成D的反应为水解反应,故D为
,红外光谱图显示D中有两个相同的官能团,且D能连续氧化,说明D中含有醇羟基,则C生成D的反应为水解反应,故D为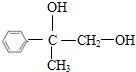 ,F为
,F为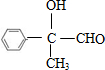 ,G为
,G为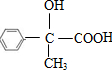 ,D在浓硫酸作用下发生脱水反应生成E,据此解答.
,D在浓硫酸作用下发生脱水反应生成E,据此解答.| 9×2+2-12 |
| 2 |
 ,则B为
,则B为 ,C为
,C为 ,红外光谱图显示D中有两个相同的官能团,且D能连续氧化,说明D中含有醇羟基,则C生成D的反应为水解反应,故D为
,红外光谱图显示D中有两个相同的官能团,且D能连续氧化,说明D中含有醇羟基,则C生成D的反应为水解反应,故D为 ,F为
,F为 ,G为
,G为 ,D在浓硫酸作用下发生脱水反应生成E,
,D在浓硫酸作用下发生脱水反应生成E, ,含氧官能团的名称是羟基,B的结构简式是:
,含氧官能团的名称是羟基,B的结构简式是: ,
, ;
; 与溴发生加成反应生成
与溴发生加成反应生成 ,
, 在氢氧化钠水溶液、加热条件下发生水解反应生成
在氢氧化钠水溶液、加热条件下发生水解反应生成 ,
, ,故答案为:
,故答案为: ;
; )含有相同官能团的同分异构体,同条件下也只得到B(
)含有相同官能团的同分异构体,同条件下也只得到B( ),A1应为
),A1应为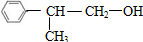 ,A1生成B的化学方程式为
,A1生成B的化学方程式为 ,
, .
.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
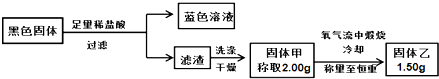
| A、只有CuO |
| B、CuO、Cu2S和CuS |
| C、CuO、CuS |
| D、CuO、Cu2S |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由石墨比金刚石稳定可知:C(金刚石,s)═C(石墨,s)△H<0 |
| B、在101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ热量,H2的燃烧热为-285.8 kJ?mol-1 |
| C、在101 kPa时,1 mol C与适量O2反应生成1 mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ?mol-1 |
| D、在稀溶液中:H+ (aq)+OH- (aq)═H2O(l)△H=-57.31 kJ?mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量等于57.31 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸 | B、硝酸钾 |
| C、氯化钡 | D、氯化铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、m+n>p |
| B、A的转化率增大 |
| C、平衡逆向移动 |
| D、C的体积百分含量增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
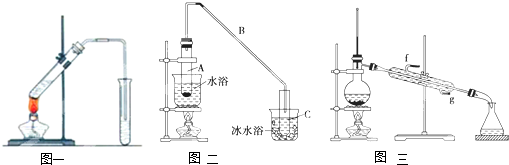
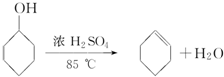
| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
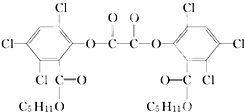 夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏.“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列有关说法不正确的是( )
夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏.“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列有关说法不正确的是( )| A、草酸二酯的分子式为C26H24Cl6O8 |
| B、1 mol草酸二酯与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗4 mol NaOH |
| C、该有机物能发生加成反应、取代反应、氧化反应 |
| D、1 mol草酸二酯与氢气完全反应,需要氢气6 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com