
·ÖĪö £Ø1£©øĆĪĀ¶ČĻĀ”¢øĆČŻĘ÷ÖŠ£¬ŌŁ¼ĢŠų¼ÓČė1molµÄSO2£Øg£©£¬Ę½ŗāÕżĻņŅĘ¶Æ£»
£Ø2£©ŌŚ10LČŻĘ÷ÖŠ£¬¼ÓČė2molµÄSO2£Øg£©ŗĶ2molµÄNO2£Øg£©£¬±£³ÖĪĀ¶Čŗć¶Ø£¬µ±“ļµ½Ę½ŗāדĢ¬Ź±£¬²āµĆČŻĘ÷ÖŠSO2£Øg£©µÄ×Ŗ»ÆĀŹĪŖ50%£¬×Ŗ»ÆµÄSO2ĪŖ2mol”Į50%=1mol£¬Ōņ£ŗ
SO2£Øg£©+NO2£Øg£©?SO3£Øg£©+NO£Øg£©
ĘšŹ¼Įæ£Ømol£©£ŗ2 2 0 0
×Ŗ»ÆĮæ£Ømol£©£ŗ1 1 1 1
Ę½ŗāĮæ£Ømol£©£ŗ1 1 1 1
ŌŁøł¾ŻK=$\frac{c£ØS{O}_{3}£©£®c£ØNO£©}{c£ØS{O}_{2}£©£®c£ØN{O}_{2}£©}$¼ĘĖćĘ½ŗā³£Źż£»
ŌŁ¼ĢŠų¼ÓČė1molµÄSO2£Øg£©£¬µČŠ§ĪŖæŖŹ¼¼ÓČė3molµÄSO2£Øg£©ŗĶ2molµÄNO2£Øg£©£¬ÉčĘ½ŗāŹ±ČŻĘ÷ÖŠSO2£Øg£©µÄÅØ¶ČŹĒxmol/L£¬±ķŹ¾³öĘäĖü×é·ÖµÄĘ½ŗāÅØ¶Č£¬ŌŁøł¾ŻĘ½ŗā³£ŹżĮŠ·½³Ģ¼ĘĖć£»
£Ø3£©SO2”¢NO2ĘšŹ¼ĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1£¬ÓÖ°“ĪļÖŹµÄĮæ1£ŗ1·“Ó¦£¬¶žÕß×Ŗ»ÆĀŹĻąµČ£¬øł¾Ż£Ø2£©¼ĘĖćæÉÖŖŠĀĘ½ŗāŹ±SO2µÄ×Ŗ»ÆĀŹ”¢NO2µÄ×Ŗ»ÆĀŹ£»
£Ø4£©Ōö“óŅ»ÖÖ·“Ó¦ĪļµÄÓĆĮ棬Ęä×Ŗ»ÆĀŹ½«¼õŠ”£¬ĮķŅ»·“Ó¦ĪļµÄ×Ŗ»ÆĀŹ½«Ōö“ó£¬ĻÖŹµÉś²śÖŠµÄŅāŅåŹĒ£ŗæÉŅŌĶعżŌö“óµĶ³É±¾ĪļÖŹµÄÓĆĮ棬Ą“Ģįø߳ɱ¾øߵķ“Ó¦ĪļµÄĄūÓĆĀŹ£®
½ā“š ½ā£ŗ£Ø1£©øĆĪĀ¶ČĻĀ”¢øĆČŻĘ÷ÖŠ£¬ŌŁ¼ĢŠų¼ÓČė1molµÄSO2£Øg£©£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬NO2µÄ×Ŗ»ÆĀŹ½«Ōö“ó£¬
¹Ź“š°øĪŖ£ŗÕż·“Ó¦£»Ōö“ó£»
£Ø2£©ŌŚ10LČŻĘ÷ÖŠ£¬¼ÓČė2molµÄSO2£Øg£©ŗĶ2molµÄNO2£Øg£©£¬±£³ÖĪĀ¶Čŗć¶Ø£¬µ±“ļµ½Ę½ŗāדĢ¬Ź±£¬²āµĆČŻĘ÷ÖŠSO2£Øg£©µÄ×Ŗ»ÆĀŹĪŖ50%£¬×Ŗ»ÆµÄSO2ĪŖ2mol”Į50%=1mol£¬Ōņ£ŗ
SO2£Øg£©+NO2£Øg£©?SO3£Øg£©+NO£Øg£©
ĘšŹ¼Įæ£Ømol£©£ŗ2 2 0 0
×Ŗ»ÆĮæ£Ømol£©£ŗ1 1 1 1
Ę½ŗāĮæ£Ømol£©£ŗ1 1 1 1
Ę½ŗāŹ±c£ØSO2£©=c£ØNO2£©=c£ØSO3£©=c£ØNO£©=$\frac{1mol}{10L}$=0.1mol/L£¬
Ę½ŗā³£ŹżK=$\frac{c£ØS{O}_{3}£©£®c£ØNO£©}{c£ØS{O}_{2}£©£®c£ØN{O}_{2}£©}$=$\frac{0.1”Į0.1}{0.1”Į0.1}$=1
ŌŁ¼ĢŠų¼ÓČė1molµÄSO2£Øg£©£¬µČŠ§ĪŖæŖŹ¼¼ÓČė3molµÄSO2£Øg£©ŗĶ2molµÄNO2£Øg£©£¬ÉčĘ½ŗāŹ±ČŻĘ÷ÖŠSO2£Øg£©µÄÅØ¶ČŹĒxmol/L£¬Ōņ£ŗ
SO2£Øg£©+NO2£Øg£©?SO3£Øg£©+NO£Øg£©
ĘšŹ¼Įæ£Ømol/L£©£ŗ0.3 0.2 0 0
×Ŗ»ÆĮæ£Ømol/L£©£ŗ0.3-x 0.3-x 0.3-x 0.3-x
Ę½ŗāĮæ£Ømol/L£©£ŗx x-0.1 0.3-x 0.3-x
ĖłŅŌ$\frac{£Ø0.3-x£©£®£Ø0.3-x£©}{x£®£Øx-0.1£©}$=1£¬½āµĆx=0.18£¬
¹Ź“š°øĪŖ£ŗ0.18£»
£Ø3£©SO2”¢NO2ĘšŹ¼ĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1£¬ÓÖ°“ĪļÖŹµÄĮæ1£ŗ1·“Ó¦£¬¶žÕß×Ŗ»ÆĀŹĻąµČ£¬¹ŹNO2µÄ×Ŗ»ÆĀŹĪŖ50%£»ŠĀĘ½ŗāŹ±SO2µÄ×Ŗ»ÆĀŹ=$\frac{0.12mol/L}{0.3mol/L}$”Į100%=40%”¢NO2µÄ×Ŗ»ÆĀŹ=$\frac{0.12mol/L}{0.2mol/L}$”Į100%=60%£»
¹Ź“š°øĪŖ£ŗ40%£»50%£»60%£»
£Ø4£©Ōö“óŅ»ÖÖ·“Ó¦ĪļµÄÓĆĮ棬Ęä×Ŗ»ÆĀŹ½«¼õŠ”£¬ĮķŅ»·“Ó¦ĪļµÄ×Ŗ»ÆĀŹ½«Ōö“ó£¬ĻÖŹµÉś²śÖŠµÄŅāŅåŹĒ£ŗæÉŅŌĶعżŌö“óµĶ³É±¾ĪļÖŹµÄÓĆĮ棬Ą“Ģįø߳ɱ¾øߵķ“Ó¦ĪļµÄĄūÓĆĀŹ£¬
¹Ź“š°øĪŖ£ŗ¼õŠ”£»Ōö“ó£»Į®¼Ū·“Ó¦Īļ£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāÓŠ¹Ų¼ĘĖć£¬Éę¼°Ę½ŗā³£Źż¼ĘĖć¼°Ó¦ÓĆ£¬²ąÖŲæ¼²éѧɜ·ÖĪö¼ĘĖćÄÜĮ¦£¬ÕĘĪÕČż¶ĪŹ½½āĢā·ØŌŚ»ÆŃ§Ę½ŗā¼ĘĖćÖŠÓ¦ÓĆ£¬×¢ŅāĘ½ŗā³£ŹżÓŠ¹ŲÓ¦ÓĆ£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
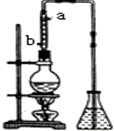 ŹŠŹŪŅŅČ©Ķس£ĪŖ40%×óÓŅµÄŅŅČ©ČÜŅŗ£®¾ĆÖƵÄŅŅČ©ČÜŅŗ»į²śÉś·Ö²ćĻÖĻó£¬ÉĻ²ćĪŖĪŽÉ«ÓĶדŅŗĢ壬ĻĀ²ćĪŖĖ®ČÜŅŗ£®¾Ż²ā¶Ø£¬ÉĻ²ćĪļÖŹĪŖŅŅČ©µÄ¼ÓŗĻĪļ£ØC2H4O£©n£¬ĖüµÄ·Šµć±ČĖ®µÄ·Šµćøߣ¬·Ö×ÓÖŠĪŽČ©»ł£®ŅŅČ©ŌŚČÜŅŗÖŠŅ×±»Ńõ»Æ£¬ĪŖ“Ó±äÖŹµÄŅŅČ©ČÜŅŗÖŠĢįČ”ŅŅČ©£ØČŌµĆµ½ČÜŅŗ£©£¬æÉĄūÓĆČēĻĀ·“Ó¦ŌĄķ£ŗ£ØC2H4O£©n$\stackrel{{H}^{+}}{”ś}$n£ØC2H4O£©
ŹŠŹŪŅŅČ©Ķس£ĪŖ40%×óÓŅµÄŅŅČ©ČÜŅŗ£®¾ĆÖƵÄŅŅČ©ČÜŅŗ»į²śÉś·Ö²ćĻÖĻó£¬ÉĻ²ćĪŖĪŽÉ«ÓĶדŅŗĢ壬ĻĀ²ćĪŖĖ®ČÜŅŗ£®¾Ż²ā¶Ø£¬ÉĻ²ćĪļÖŹĪŖŅŅČ©µÄ¼ÓŗĻĪļ£ØC2H4O£©n£¬ĖüµÄ·Šµć±ČĖ®µÄ·Šµćøߣ¬·Ö×ÓÖŠĪŽČ©»ł£®ŅŅČ©ŌŚČÜŅŗÖŠŅ×±»Ńõ»Æ£¬ĪŖ“Ó±äÖŹµÄŅŅČ©ČÜŅŗÖŠĢįČ”ŅŅČ©£ØČŌµĆµ½ČÜŅŗ£©£¬æÉĄūÓĆČēĻĀ·“Ó¦ŌĄķ£ŗ£ØC2H4O£©n$\stackrel{{H}^{+}}{”ś}$n£ØC2H4O£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ¼ĖįøĘŌŚĖ®ÖŠČܽā¶ČŗÜŠ”£¬ĘäČÜŅŗµÄµē×čĀŹŗÜ“ó£¬ĖłŅŌĢ¼ĖįøĘŹĒČõµē½āÖŹ | |
| B£® | Ģ¼ĖįøĘŌŚĖ®ÖŠµÄČܽā¶ČŗÜŠ”£¬µ«±»ČܽāµÄĢ¼ĖįøĘČ«²æµēĄė£¬ĖłŅŌĢ¼ĖįøĘŹĒĒæµē½āÖŹ | |
| C£® | ĀČĘųŗĶ°±ĘųµÄĖ®ČÜŅŗµ¼µēŠŌ¶¼ŗÜŗĆ£¬ĖłŅŌĖüĆĒŹĒĒæµē½āÖŹ | |
| D£® | Ė®ÄѵēĄė£¬“æĖ®¼øŗõ²»µ¼µē£¬ĖłŅŌĖ®ŹĒ·Ēµē½āÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĪļÖŹĆū³Ę | ŗģĮ×Óė°×Į× | øżĶéÓėŹ®ĮłĶé | ĀČ·ĀÓėČżĀČ¼×Ķé | ėÓėė®”¢ė° | ŠĀĪģĶéÓė2£¬2-¶ž¼×»ł¶”Ķé | 2-¼×»łĪģĶéÓė2£¬3-¶ž¼×»ł¶”Ķé |
| Ļą»„¹ŲĻµ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
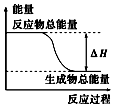
| A£® | ĀĮ·ŪÓėŃõ»ÆĢśŌŚ¼ÓČČĢõ¼žĻĀµÄ·“Ó¦ | |
| B£® | ×ĘČȵÄĢ¼Óė¶žŃõ»ÆĢ¼·“Ó¦ | |
| C£® | Ba£ØOH£©2•8H2O¾§ĢåŗĶNH4Cl¾§Ģå»ģŗĻ | |
| D£® | Ģ¼ÓėĖ®øßĪĀĢõ¼žĻĀÖĘČ”Ė®ĆŗĘųµÄ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
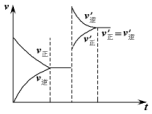 ČēĶ¼±ķŹ¾ŌŚĆܱÕČŻĘ÷ÖŠ·“Ó¦C£Øs£©+H2O£Øg£©$\stackrel{øßĪĀ}{?}$CO£Øg£©+H2£Øg£©£»”÷H£¾0£¬“ļµ½Ę½ŗāŗó£¬ÓÉÓŚĢõ¼žµÄøıä¶ųŅżĘšÕż”¢Äę·“Ó¦ĖŁĀŹµÄ±ä»Æ£¬ŅŌ¼°Ę½ŗāŅĘ¶ÆµÄדæö£®¾ŻĶ¼æÉÖŖ£¬øıäµÄĢõ¼žŹĒ£Ø””””£©
ČēĶ¼±ķŹ¾ŌŚĆܱÕČŻĘ÷ÖŠ·“Ó¦C£Øs£©+H2O£Øg£©$\stackrel{øßĪĀ}{?}$CO£Øg£©+H2£Øg£©£»”÷H£¾0£¬“ļµ½Ę½ŗāŗó£¬ÓÉÓŚĢõ¼žµÄøıä¶ųŅżĘšÕż”¢Äę·“Ó¦ĖŁĀŹµÄ±ä»Æ£¬ŅŌ¼°Ę½ŗāŅĘ¶ÆµÄדæö£®¾ŻĶ¼æÉÖŖ£¬øıäµÄĢõ¼žŹĒ£Ø””””£©| A£® | Ōö¼ÓCOÅØ¶Č | B£® | ÉżøßĪĀ¶Č | C£® | Ōö¼ÓĖ®ÕōĘų | D£® | Ōö“óŃ¹Ēæ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com