
(14)A、B、C、D、E、F是常见单质,其中A是用量最大,应用最广泛的金属;元素D是地壳中含量最多的金属元素;D元素和E元素在周期表中相邻。G、H、I、J、K、L是常见化合物,其中G在常温下是无色液体,H是黑色固体。以上物质相互间的转化关系如图所示: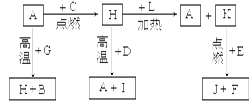
请回答下列问题:
(1)元素A在元素周期表中的位置为 周期 族。
(2)写出K的电子式 。
(3)写出H和D反应的化学方程式 。
(4)D能与氢氧化钠溶液反应,请写出该反应的离子方程式 。
(5)写出A与G反应的化学方程式 。
(6)K与E反应时产生的现象有 ;该反应的化学方程式为 ___________________。
(7)已知F的燃烧热为akJ/mol,L的燃烧热为bkJ/mol,试写出F生成L的热化学方程式_________________
(1)四;VIII ;(2) ;(3)3Fe3O4+8Al
;(3)3Fe3O4+8Al 4Al2O3+9Fe
4Al2O3+9Fe
(4)2Al+2OH-+2H2O==2AlO2-+3H2↑ (5)3Fe+4H2O(g) Fe3O4+4H2↑
Fe3O4+4H2↑
(6)镁带剧烈燃烧,放出耀眼的光,瓶壁出现白色固体和黑色颗粒;2Mg+CO2 2MgO+C
2MgO+C
(7) C(s)+ 1/2O2(g) CO (g) ΔH=-(a-b)kJ/mol;
CO (g) ΔH=-(a-b)kJ/mol;
解析试题分析:根据题意及物质间的转化关系可得:A是Fe;B是H2;C是O2;D是Al;E是Mg;F是C;G是H2O;H是Fe3O4;I是Al2O3;J是MgO;K是CO2;L是CO。(1)26号元素Fe在元素周期表中位于第四周期第VIII族;(2)CO2的电子式是 ;(3)Fe3O4和Al发生铝热反应的化学反应方程式是3Fe3O4+8Al
;(3)Fe3O4和Al发生铝热反应的化学反应方程式是3Fe3O4+8Al 4Al2O3+9Fe;(4)Al与氢氧化钠溶液反应的离子方程式是2Al+2OH- +2H2O= 2AlO2- +3H2↑;(5)炽热的Fe与水蒸气反应的化学方程式是3Fe+4H2O(g)
4Al2O3+9Fe;(4)Al与氢氧化钠溶液反应的离子方程式是2Al+2OH- +2H2O= 2AlO2- +3H2↑;(5)炽热的Fe与水蒸气反应的化学方程式是3Fe+4H2O(g) Fe3O4+4H2;(6)Mg带在CO2中能够着火剧烈燃烧,放出耀眼的光,瓶壁出现白色固体和黑色颗粒;反应的化学方程式为2Mg+CO2
Fe3O4+4H2;(6)Mg带在CO2中能够着火剧烈燃烧,放出耀眼的光,瓶壁出现白色固体和黑色颗粒;反应的化学方程式为2Mg+CO2 2MgO+C;(7)根据题意可得热化学方程式①C(s)+ O2(g)
2MgO+C;(7)根据题意可得热化学方程式①C(s)+ O2(g) CO2(g) ΔH="-akJ/mol;" ②CO(g)+ 1/2O2(g)
CO2(g) ΔH="-akJ/mol;" ②CO(g)+ 1/2O2(g) CO2(g) ΔH="-bkJ/mol" bkJ/mol, ①-②整理可得:C(s)+ 1/2O2(g)
CO2(g) ΔH="-bkJ/mol" bkJ/mol, ①-②整理可得:C(s)+ 1/2O2(g) CO (g) ΔH=-(a-b)kJ/mol;
CO (g) ΔH=-(a-b)kJ/mol;
考点:考查元素及化合物的推断、电子式、化学方程式、离子方程式及热化学方程式的书写的知识。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:单选题
将11.9 g由Mg、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7 g。另取等质量的合金溶于过量稀硝酸中,生成了6.72 L NO(标准状况下),向反应后的溶液中加入适量NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,则沉淀的质量为
| A.22.1 g | B.27.2 g | C.30 g | D.无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各项表达中,正确的是
A.水的电子式为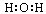 |
| B.将58g等体积的乙烯和乙烷混合物完全燃烧,生成的二氧化碳体积为89.6L |
| C.所有的氮原子中,质子数都是7个,但不一定是相同的原子 |
D.氯离子的结构示意图为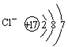 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(6分)用9mol/L的浓硫酸稀释成 0.9mol/L的稀硫酸 100mL ,回答下列问题:
(1)配制操作可分解成如下几步,以下正确的操作顺序是_____________________
A 向容量瓶中注入少量蒸馏水,检查是否漏水
B 用少量蒸馏水洗涤烧杯及玻璃棒,将溶液注入容量瓶,并重复操作两次
C 用已冷却的稀硫酸注入已检查不漏水的容量瓶中
D 根据计算,用量筒量取一定体积的浓硫酸
E.将浓硫酸沿烧杯壁慢慢注入盛有蒸馏水的小烧杯中,并不断用玻璃棒搅拌
F.盖上容量瓶塞子,振荡,摇匀
G.用胶头滴管滴加蒸馏水,使溶液凹面恰好与刻度相切
H.继续往容量瓶中小心地加蒸馏水,使液面接近刻度线1~2 cm
(2)如果实验室用98%的浓硫酸(密度为1.8g·cm-3 ) 配制3. 6 mol·L-1的稀硫酸250mL。计算所需浓硫酸的体积为_____________mL。
(3)由于错误操作, 使得到的浓度数据比正确的偏大的是___________(填写序号)。
A 使用容量瓶配制溶液时, 俯视液面定容后所得溶液的浓度
B 没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中
C 容量瓶用蒸馏水洗净,没有烘干
D 定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
E.把配好的溶液倒入用蒸馏水洗净而未干的试剂瓶中备用
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
将4molA气体和2molB气体在2L的密闭容器中混合,在一定条件下发生如下反应:
2A(g)+B(g) 2C(g)若经过2秒后测得C的浓度为0.6mol/L。
2C(g)若经过2秒后测得C的浓度为0.6mol/L。
则:(1)2s内用B表示的反应速率 。
(2)2s时A的物质的量浓度为 。
(3)2s时B的物质的量为 。
(4)最终C的浓度 (填“能”或“不能”)达到2mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某氮肥NH4HCO3中混有少量(NH4)2CO3,现采用下列方案测定该氮肥中(NH4)2CO3的质量分数:称取5.7 g样品与2.0 mol·L-1 NaOH溶液混合,完全溶解后,低温加热使其充分反应(该温度下铵盐不分解),并使生成的氨气全部被硫酸吸收,测得氨气的质量与所用NaOH溶液体积的关系如图所示。请回答下列问题: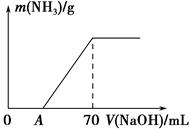
(1)A点前样品与NaOH反应的离子方程式为 。
(2)为使生成的氨气被硫酸吸收时不发生倒吸,可以选用下列装置中的 (填字母序号)。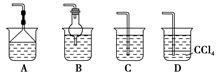
(3)样品中(NH4)2CO3的质量分数是 %(保留一位小数)。
(4)当V(NaOH)=50 mL时,生成NH3的质量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
“84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶某品牌“84消毒液”,
并查阅相关资料和消毒液包装说明得到如下信息:
“84消毒液”:含25% NaClO、1 000 mL、密度1.19 g·cm-3,稀释100倍(体积比)后使用。请根据以上信息和相关知识回答下列问题:
(1)该“84消毒液”的物质的量浓度为________mol·L-1。
(2)该同学取100 mL该品牌“84消毒液”稀释后用于消毒,稀释后的溶液中c(Na+ )≈________mol·L-1(假设稀释后溶液密度为1.0 g·cm-3)。
(3)该同学参阅该品牌“84消毒液”的配方,欲用NaClO固体配制480 mL含25% NaClO的消毒液。下列说法正确的是________。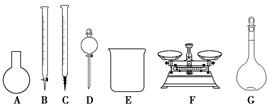
| A.如图所示的仪器中,有四种是不需要的,还需一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干才能用于溶液配制 |
| C.利用购买的商品NaClO来配制可能导致结果偏低 |
| D.需要称量的NaClO固体质量为143 g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
根据下面物质间转化的框图,回答有关问题;
`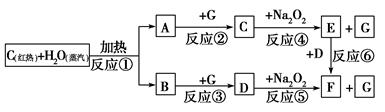
(1)由反应①产生的A、B混合物的工业名称是________。
(2)写出框图中D、E的化学式:D________;E________。
(3)如果2 mol Na2O2与足量水蒸气反应,可得标准状况下气体的体积是________L,同时反应中转移电子总数是____________。(NA表示阿伏加德罗常数)
(4)如果A、B混合气体7.8 g,在与G充分反应后,通过足量Na2O2层,可使Na2O2增重________g。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(Ⅰ)在室温下,向某一容积固定的真空容器内充入丁烷(气)和氧气,使容器内混合气的总压强达到p1,点火燃烧,氧气反应完全,冷却至室温后容器内气体的总压强为p2。
(1)若丁烷燃烧的生成物只有H2O(液)和CO2,则p2/p1= 。
(2)若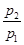 =0.64,则反应前混合气中丁烷的物质的量分数= 。
=0.64,则反应前混合气中丁烷的物质的量分数= 。
(Ⅱ)设阿伏加德罗常数为NA,在常温常压下气体的摩尔体积为Vm L·mol-1,O2和N2的混合气体a g含有b个分子,则c g该混合气体在常温常压下所占的体积应是 L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com