
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
(1)处理NOx的一种方法是利用甲烷催化还原NOx.已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=﹣574kJ•mol﹣1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=﹣1160kJ•mol﹣1
则甲烷直接将NO2还原为N2的热化学方程式为 .
(2)利用反应6NO2+8NH3 7N2+12H2O处理NO2.当转移1.2mol电子时,消耗的NO2在标准状况下是 L.NO2也可用NaOH溶液吸收,生成两种盐,该反应的化学方程式为: .
7N2+12H2O处理NO2.当转移1.2mol电子时,消耗的NO2在标准状况下是 L.NO2也可用NaOH溶液吸收,生成两种盐,该反应的化学方程式为: .
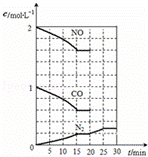
(3)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:2NO(g)+2CO(g)⇌N2(g)+2CO2(g);△H<0.该反应的化学平衡常数表达式为K= 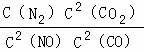 ,该反应△S 0(填“>”或“<”)若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示.若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将 移动(填“向左”、“向右”或“不”).20min时,若改变反应条件,导致N2浓度发生如图所示的变化,则改变的条件可能是 (填序号).
,该反应△S 0(填“>”或“<”)若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示.若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将 移动(填“向左”、“向右”或“不”).20min时,若改变反应条件,导致N2浓度发生如图所示的变化,则改变的条件可能是 (填序号).
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的量
(4)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42﹣而实现SO2的处理(总反应为2SO2+O2+2H2O=2H2SO4).已知,含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,则另一反应的离子方程式为 .
| 用盖斯定律进行有关反应热的计算;氧化还原反应的计算;化学平衡常数的含义;化学平衡的影响因素. | |
| 专题: | 氧化还原反应专题;化学反应中的能量变化;化学平衡专题. |
| 分析: | (1)利用盖斯定律分析,不管化学反应是一步或分几步完成,其反应热是不变的;依据热化学方程式和盖斯定律构造目标热化学方程式并计算反应热; (2)根据化合价的变化结合方程式计算;NaOH溶液吸收NO2,生成两种盐,二氧化氮被氧化生成硝酸根离子; (3)依据平衡常数概念列式计算,△S表示反应的熵变,依据浓度商和平衡常数比较分析判断; (4)SO2转化为SO42﹣该过程为氧气氧化二价铁离子到三价铁离子,然后用三价铁离子氧化二氧化硫到硫酸根离子,据此写出反应的离子方程式. |
| 解答: | 解:(1)①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=﹣574kJ•mol﹣1 ②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=﹣1160kJ•mol﹣1 由盖斯定律计算(①+②)× 故答案为:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ•mol﹣1; (2)反应6NO2+8NH3 NaOH溶液吸收NO2,生成两种盐,二氧化氮被氧化生成硝酸根离子,同时二氧化氮被还原生成亚硝酸根离子,反应方程式为:2NO2+2NaOH=NaNO3+NaNO2+H2O, 故答案为:6.72L 2NO2+2NaOH=NaNO3+NaNO2+H2O; (3)反应方程式2NO(g)+2CO(g)⇌2CO2(g)+N2(g)的化学平衡常数表达式为:K= △S表示反应的熵变,该反应为气体体积减小的反应,所以△S<0, 依据图象分析,15分钟时达到平衡时氮气浓度为0.2mol/L,NO平衡浓度为1.6mol/L,一氧化碳浓度为0.6mol/L,二氧化碳浓度为0.4mol/L,2NO(g)+2CO(g)⇌N2(g)+2CO2(g)△H<0;平衡常数K= 20min时,若改变反应条件,导致N2浓度发生如图1所示的变化,斜率减小反应速率减小,氮气浓度增大,反应是气体体积减小的放热反应,则改变的条件可能是降温, 故答案为: (4)常温下将SO2转化为SO42﹣而实现SO2的处理.含SO2的废气通入含Fe2+、Fe3+的溶液时其中一个反应的离子方程式为:4Fe2++O2+4H+═4Fe3++2H2O,则另一反应的离子方程式为三价铁离子氧化二氧化硫到硫酸根离子,反应的离子方程式为:2Fe3++SO2+2H20=2Fe2++SO42﹣+4H+, 故答案为:2Fe3++SO2+2H2O=2Fe2++SO42﹣+4H+. |
| 点评: | 本题考查了反应热的计算、化学反应速率与化学平衡图象的综合利用、化学平衡常数的计算、氧化还原反应方程式的书写等知识,题目难度较大,试题的计算量较大,涉及的知识点较多,充分考查了学生的分析、理解能力及灵活应用所学知识的能力,(3)为难点,注意先计算出化学平衡常数,然后再根据浓度商判断平衡移动方向. |


科目:高中化学 来源: 题型:
(1)中学教材中图示了NaCl晶体,它向三维空间延伸得到完美晶体。NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近的O2-核间距离为a×10-8cm,计算NiO晶体的密度。(已知NiO的摩尔质量为74.7 g·mol-1)

(2)天然和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另两个Ni2+被两个Ni3+所取代。其结果晶体仍呈电中性,但化合物Ni和O的比值却发生了变化。某氧化镍样品的组成为Ni0.97O,试计算晶体中Ni3+与Ni2+的离子个数之比。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y和W为原子序数依次递增的短周期元素,X和Y同主族,Y和W的氢化物具有相同的电子数。在中学范围内X的单质只有氧化性,且是空气的主要成份之一。
(1)写出实验室制取W2反应的离子方程式 。
(2)某小组设计如图所示的装置,分别研究YX2和W2的性质。
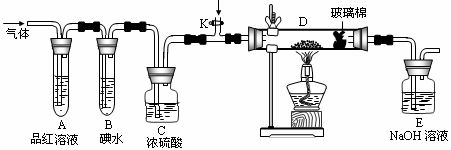
①分别通入YX2和W2,在装置A中观察到的现象是否相同 (填“相同”或“不相同”);若装置D中装的是铁粉,当通入足量W2时观察到的现象为 ;若装置D中装的是五氧化二钒,当通入足量YX2时,打开K通入适量X2,化学反应方程式为 ;
②若装置B中装有5.0mL 1.0×10-3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,该反应的化学方程式为 。
(3)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成,再向该试管中加入过量的下列溶液也无沉淀生成的是 (填字母)。
A.氨水 B.稀盐酸 C.稀硝酸 D.氯化钙 E.双氧水 F.硝酸银
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下发生反应:2A(g)+2B(g)⇌xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率VD=0.2mol/(L•min),下列说法正确的是( )
|
| A. | A和B的转化率均是20% |
|
| B. | x=4 |
|
| C. | 平衡时A的物质的量为2.8mol |
|
| D. | 平衡时气体压强比原来减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在一个2L的密闭容器中,加入4mol A和2mol B进行如下反应:3A(g)+2B(g)⇌4C(l)+2D(g),反应一段时间后达到平衡,测得生成1.6mol C,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
|
| A. | 该反应的化学平衡常数表达式是K= |
|
| B. | 此时,B的平衡转化率是35% |
|
| C. | 增大该体系的压强,平衡向右移动,化学平衡常数增大 |
|
| D. | 增加C,B的平衡转化率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下面三个数据:①7.2×10-4 ②4.6×10-4 ③4.9×10-10,分别是三种酸的电离平衡常数,若已知这些酸可发生如下反应:NaCN+HNO2===HCN+NaNO2;NaCN+HF===HCN+NaF;NaNO2+HF===HNO2+NaF。由此可判断下列叙述中,正确的是( )
A.HF的电离平衡常数是①
B.HNO2的电离平衡常数是①
C.HCN的电离平衡常数是②
D.HNO2的电离平衡常数是③
查看答案和解析>>
科目:高中化学 来源: 题型:
欲使0.1mol·L-1的NaHCO3溶液中c(H+)、c(CO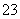 )、c(HCO
)、c(HCO )都减少,其方法是( )
)都减少,其方法是( )
A.通入二氧化碳气体
B.加入氢氧化钠固体
C.通入氯化氢气体
D.加入饱和石灰水溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实与氢键无关的是( )
A.液态氟化氢中有三聚氟化氢(HF)3分子存在
B.冰的密度比液态水的密度小
C.乙醇能与水以任意比混溶而甲醚(CH3—O—CH3)难溶于水
D.H2O比H2S稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
表示阿伏加德罗常数,下列叙述中正确的是
A.标准状况下,2.24L三氯甲烷含有分子数目为0.1
B.1 mol FeI2与足量氯气反应转移的电子数为2
C.1 molCH3COONa 和少量CH3COOH溶于水所得中性溶液中,CH3COO-数目为
D.标准状况下,22.4L的乙烯中含有的共用电子对数为12
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com