
【题目】下列说法正确的是( )
A.同种元素的质子数必定相同
B.不同元素原子的质量数必定不同
C.原子核都是由质子和中子构成的
D.凡是核外电子数相同的微粒必定属于同一元素
科目:高中化学 来源: 题型:
【题目】用酒精灯加热时,需要垫石棉网的仪器有 ( )
① 烧杯 ② 坩埚 ③ 锥形瓶 ④ 蒸发皿 ⑤ 试管 ⑥ 烧瓶
A.②④⑤B.①②③C.④⑤⑥D.①③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NA代表阿伏加德罗常数的数值,则关于热化学方程式C2H2(g)+![]() O2(g)===2CO2(g)+H2O(l) ΔH=-1300 kJ·mol-1的说法中,正确的是( )
O2(g)===2CO2(g)+H2O(l) ΔH=-1300 kJ·mol-1的说法中,正确的是( )
A. 转移10NA个电子时,该反应放出1300 kJ的能量
B. 生成NA个液态水分子时,吸收1300 kJ的能量
C. 有2NA个碳氧共用电子对生成时,放出1300 kJ的能量
D. 有10NA个碳氧共用电子对生成时,放出1300 kJ的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应 2SO2(g) + O2(g)![]() 2SO3(g)(正反应放热),相关数据如下,下列说法正确的是( )
2SO3(g)(正反应放热),相关数据如下,下列说法正确的是( )
容器 1 | 容器 2 | 容器 3 | |
反应温度 T/K | 700 | 700 | 800 |
反应物投入量 | 2molSO2、 1molO2 | 4molSO3 | 2molSO2、 1molO2 |
平衡ν正(SO2 )/mol·L-1·s-1 | ν1 | ν2 | ν3 |
平衡 c(SO3 )/ mol·L-1 | c1 | c2 | c3 |
平衡体系总压强 p/Pa | p1 | p2 | p3 |
物质的平衡转化率ɑ | α1(SO2) | α2(SO3) | α3(SO2) |
平衡常数 K | K1 | K2 | K3 |
A. ν1<ν2,c2<2c1 B. K1>K3,p2>2p3
C. ν1< ν3,α1(SO2) > α3(SO2) D. c2>2c3,α2(SO3) +α3(SO2)<1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)真空碳热还原-氧化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g) △H=akJ·mol-1
3AlCl(g)═2Al(l)+AlCl3(g) △H=bkJ·mol-1
反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=________kJ·mol-1(用含a、b的代数式表示);
(2)已知 2SO2(g)+O2(g)=2SO3(g)△H反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3放出99kJ的热量,请回答下列问题:
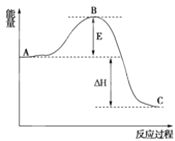
①图中A分别表示______________;
②E的大小对该反应的反应热_________(填“有”或“无”)影响;
③该反应通常用V2O5作催化剂,加V2O5会使图中B点 __________(填“升高”“降低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资源的高效利用对保护环境、促进经济持续健康发展具有重要作用。某工厂以酸性工业废水(含H+、Al3+、Mg2+、Cr2O72—、SO42—)以及硫酸厂废气(SO2)为原料提取铬的工艺流程如下:
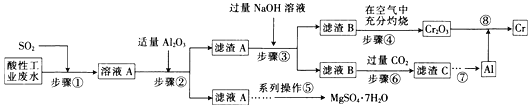
有关数据如下表所示。
化合物 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
完全沉淀的pH | 10.5 | 4.3 | 5.3 |
开始溶解的pH | — | 7.8 | 9.2 |
Ksp近似值 | 5.6×10-12 | 1.3×10-33 | 6.3×10-31 |
请回答下列问题:
(1)步骤①中发生主要反应的离子方程式为__________________________。
(2)步骤②中加入适量Al2O3的目的是__________________________。
(3)为了达到实验目的,步骤③中加入NaOH溶液,应调节溶液的pH范围为_________。
(4)步骤⑥向滤液B中通入过量CO2,反应的离子方程式为__________________________。
(5)工业上也常采用下列装置,利用电解法处理含铬废水。
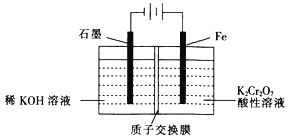
①在电解过程中阳极区pH增大的原因是_______________________。
②理论上每处理含1 mol K2Cr2O7的废水,阴极区得到的气体体积为_________(标准状况)L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关化学史的,下列说法中不正确的是
A. 道尔顿——提出原子学说 B. 爱迪生——发现电子
C. 卢瑟福——提出带核的结构模型 D. 玻尔——提出了电子在核外的量子化轨道
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com