
| A. | 铜粉中混有铁粉:加入过量盐酸充分反应,过滤 | |
| B. | CO2中混有HCl:将其通入NaOH溶液,洗气 | |
| C. | NaHCO3溶液中混有少量Na2CO3:往该溶液中通入过量CO2气体 | |
| D. | FeCl2溶液中混有少量FeCl3:加入Fe粉 |
分析 A.Fe与盐酸反应,而Cu不能;
B.二者均与NaOH溶液反应;
C.碳酸钠溶液与二氧化碳反应生成碳酸氢钠;
D.Fe与氯化铁反应生成氯化亚铁.
解答 解:A.Fe与盐酸反应,而Cu不能,则加入过量盐酸充分反应,过滤可除杂,故A正确;
B.二者均与NaOH溶液反应,不能除杂,应选碳酸氢钠溶液、洗气,故B错误;
C.碳酸钠溶液与二氧化碳反应生成碳酸氢钠,则往该溶液中通入过量CO2气体可除杂,故C正确;
D.Fe与氯化铁反应生成氯化亚铁,则加入Fe粉、过滤可除杂,故D正确;
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:选择题
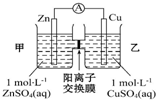
| A. | 铜电极上发生反应Cu-2e-=Cu2+ | |
| B. | 电池工作一段时间后,乙池的c(SO42- )减小 | |
| C. | 电子从锌极经过导线移向铜极 | |
| D. | 电池工作一段时间后,甲池的c(Zn2+ )增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤⑧ | B. | ②④⑤⑦⑧ | C. | ④⑤⑧ | D. | ③④⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+H+ AlO2- SO32- | B. | NH4+ Al3+SO42-Cl- | ||
| C. | OH- K+ SO42- HCO3- | D. | Fe2+Na+ ClO-NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.5 g | B. | 810 g | C. | 1250 g | D. | 900 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠不能用于治疗胃溃疡病人的胃酸过多症 | |
| B. | 切开的金属Na暴露在空气中,光亮表面会逐渐变暗 | |
| C. | 发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔 | |
| D. | 金属镁在空气中燃烧的产物是纯净的氧化镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色 | |
| B. | 有机物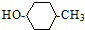 在强碱的醇溶液中可以发生消去反应 在强碱的醇溶液中可以发生消去反应 | |
| C. | 有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2=CH-COOCH3 | |
| D. | 可用新制Cu(OH)2悬浊液鉴别甲酸、乙酸、甲酸乙酯、乙酸甲酯这四种物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com