
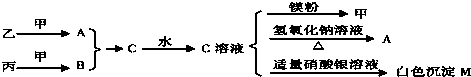
��12�֣�����ͼ��ʾ��ת����ϵ�У���֪A���ɶ�����Ԫ����ɵ���ʽ�Ρ�ͨ��״���£�D��E��F��Y��HΪ���塣G��K��Ϊ������ǿ�ᣬD��X�ķ����о�����10�����ӡ���ش��������⣺
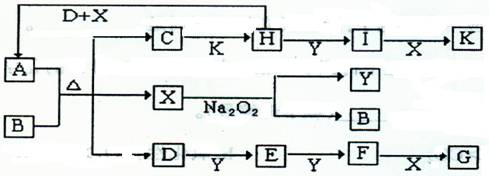
��1��B�ĵ���ʽΪ �����к��еĻ�ѧ�������� ��C�Ļ�ѧʽ�� ��
��2��д���ڼ��������£�A��������B��Һ��Ӧ�����ӷ���ʽ�� ��
��3��д��D��Y�ڵ�ȼ�����·�Ӧ������X��һ�ֵ��ʵĻ�ѧ����ʽ�� ��
��4����G��ϡ��Һ�ܽ���a mol Fe����E��Ψһ�Ļ�ԭ�������Һ�����ֽ��������ӵ����ʵ���ǡ����ȣ���ԭ��G�� mol���ú�a�Ĵ���ʽ��ʾ����
 ����ѧ���ʱѧ����ϵ�д�
����ѧ���ʱѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
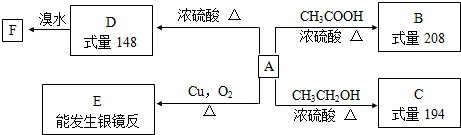
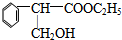
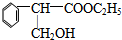
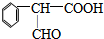
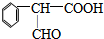
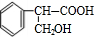
| Ũ���� |
| �� |
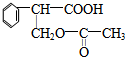 +H2O
+H2O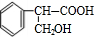
| Ũ���� |
| �� |
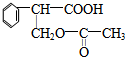 +H2O
+H2O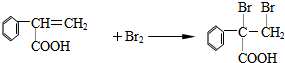
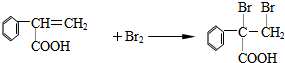
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
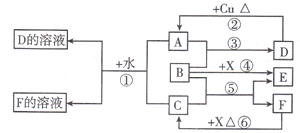
 ������A��B��C��D��E��F��G��H�����л����������ͼ��ʾ��ת����ϵ��
������A��B��C��D��E��F��G��H�����л����������ͼ��ʾ��ת����ϵ��
| ��� | �� | �� | �� | �� | �� |
| ����Ӧ�� | NaOH��Һ | ���� | ����Cu��OH��2 | ϡ���� | H2O |
| ��Ӧ���� | ���� | - | ���� | ���� | ���� HgSO4 |
| ���� |
| ���� |




�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
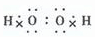
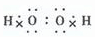
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com