


科目:高中化学 来源: 题型:
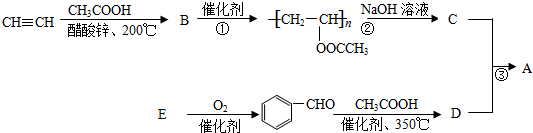
| 催化剂、350℃ |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
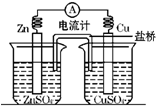
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、相对分子质量相同的物质一定是同种物质 |
| B、相对分子质量相同的不同物质一定是同分异构体 |
| C、白磷和红磷互为同分异构体 |
| D、分子式相同的不同物质一定互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将水加热到120℃,pH=6:c(OH-)<c(H+) |
| B、醋酸与醋酸钠的pH=7的混合溶液中:c(CH3COO-)>c(Na+) |
| C、0.lmoI?L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+) |
| D、pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
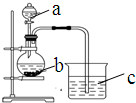 某同学想探究硫和碳原子的得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验,请回答:
某同学想探究硫和碳原子的得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com