
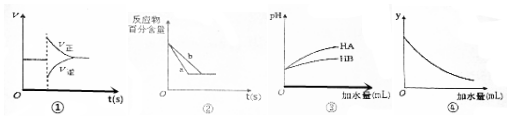
| A£® | Ķ¼¢Ł±ķŹ¾ŌŚN2£Øg£©+3H2£Øg£©?2NH3£Øg£©“ļµ½Ę½ŗāŗ󣬼õÉŁNH3ÅØ¶ČŹ±ĖŁĀŹµÄ±ä»Æ | |
| B£® | Ķ¼¢ŚÖŠa”¢bĒśĻß·Ö±š±ķŹ¾·“Ó¦H2£Øg£©+I2£Øg£©?2HI£Øg£©ŌŚÓŠ“߻ƼĮŗĶĪŽ“߻ƼĮ“ęŌŚĻĀ½ØĮ¢Ę½ŗāµÄ¹ż³Ģ | |
| C£® | Ķ¼¢ŪĖµĆ÷HBŹĒ±ČHAøüČõµÄĖį | |
| D£® | Ķ¼¢ÜÖŠµÄy±ķŹ¾½«±ł“×Ėį¼ÓĖ®Ļ”ŹĶŹ±ČÜŅŗµ¼µēÄÜĮ¦µÄ±ä»ÆĒéæö |
·ÖĪö A£®¼õÉŁNH3ÅØ¶Č£¬ÕżÄę·“Ó¦ĖŁĀŹ¶¼¼õŠ”£»
B£®H2£Øg£©+I2£Øg£©?2HI£Øg£©·“Ó¦Ē°ŗóĢå»ż²»±ä£¬ŌņŌö“óŃ¹Ēæ£¬Ę½ŗā²»ŅĘ¶Æ£»
C£®µČpHŹ±£¬øüČõµÄĖįÅضČøü“ó£¬Ļ”ŹĶĻąĶ¬±¶Źż£¬pH±ä»Æ½ĻŠ”£®
D£®½«±ł“×Ėį¼ÓĖ®Ļ”ŹĶŹ±£¬ČÜŅŗµ¼µēÄÜĮ¦ĻČŌöĒæŗó¼õČõ£®
½ā“š ½ā£ŗA£®¼õÉŁNH3ÅØ¶Č£¬Õż·“Ó¦ĖŁĀŹ²»æÉÄÜŌö“ó£¬ÕżÄę·“Ó¦ĖŁĀŹ¶¼¼õŠ”£¬ĒŅĘ½ŗāÕżĻņŅĘ¶Æ£¬¹ŹA“ķĪó£»
B£®H2£Øg£©+I2£Øg£©?2HI£Øg£©·“Ó¦Ē°ŗóĢå»ż²»±ä£¬ŌņŌö“óŃ¹Ēæ£¬Ę½ŗā²»ŅĘ¶Æ£¬²»Ņ»¶ØĪŖ“߻ƼĮ£¬¹ŹB“ķĪó£»
C£®µČpHŹ±£¬øüČõµÄĖįÅضČøü“ó£¬Ļ”ŹĶĻąĶ¬±¶Źż£¬pH±ä»Æ½ĻŠ”£¬ŌņĶ¼¢ŪĖµĆ÷HBŹĒ±ČHAøüČõµÄĖį£¬¹ŹCÕżČ·£®
D£®½«±ł“×Ėį¼ÓĖ®Ļ”ŹĶŹ±£¬ČÜŅŗµ¼µēÄÜĮ¦ĻČŌöĒæŗó¼õČõ£¬Ķ¼ĻóÓ¦ĪŖ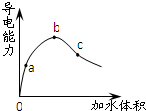 £¬¹ŹD“ķĪó£®
£¬¹ŹD“ķĪó£®
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖĶ¼Ļó·ÖĪö£¬ĪŖøßĘµæ¼µć£¬²ąÖŲ漲鷓ӦÄÜĮæ±ä»Æ£¬Ėį¼īÖŠŗĶČÜŅŗĖį¼īŠŌÅŠ¶Ļ£¬Čõµē½āÖŹĻ”ŹĶČÜŅŗÖŠĄė×ÓÅØ¶Č±ä»Æ·ÖĪö£¬ĢāÄæÄѶČÖŠµČ£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| t”ę | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ij֊ŠŌČÜŅŗÖŠ£ŗFe3+”¢Na+”¢SO42-”¢Cl- | |
| B£® | 1.2mol•L-1µÄNaNO3ČÜŅŗ£ŗFe2+”¢H+”¢Cl-”¢SO42-”¢ | |
| C£® | 0.1 mol•L-1µÄNH4HCO3ČÜŅŗ£ŗNa+”¢K+”¢NO3-”¢Cl- | |
| D£® | ÓėĀĮ·“Ó¦²śÉś“óĮæĒāĘųµÄČÜŅŗ£ŗNO3-”¢HCO3-”¢K+”¢Na+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 A”¢B”¢C”¢D”¢E·Ö±šŹĒĢś»ņĢśµÄ»ÆŗĻĪļ£¬ĘäÖŠDŹĒŅ»ÖÖŗģŗÖÉ«³Įµķ£¬ĘäĻą»„·“Ó¦¹ŲĻµČēĶ¼ĖłŹ¾£ŗ
A”¢B”¢C”¢D”¢E·Ö±šŹĒĢś»ņĢśµÄ»ÆŗĻĪļ£¬ĘäÖŠDŹĒŅ»ÖÖŗģŗÖÉ«³Įµķ£¬ĘäĻą»„·“Ó¦¹ŲĻµČēĶ¼ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ö»ÓŠ¢Ł | B£® | ¢Ł¢Ū¢Ü | C£® | ¢Ü¢Ż¢Ž | D£® | ¢Ł¢Ü¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃé²Ł×÷ | ĻÖĻó | ½įĀŪ |
| A | ³£ĪĀĻĀ½«ĀĮʬ·ÅČėÅØH2SO4ÖŠ | Éś³É“Ģ¼¤ŠŌĘųĪ¶ĘųĢå | AlŌŚ³£ĪĀĻĀÓėÅØH2SO4·“Ӧɜ³ÉSO2 |
| B | ĻņAlCl3ČÜŅŗÖŠµĪ¼Ó¹żĮæ°±Ė® | Éś³É°×É«½ŗדĪļÖŹ | Al£ØOH£©3²»ČÜÓŚ°±Ė® |
| C | ĻņijČÜŅŗÖŠ¼ÓČėKSCNČÜŅŗ£¬ŌŁĻņČÜŅŗÖŠ¼ÓČėŠĀÖĘĀČĖ® | ČÜŅŗĻČ²»ĻŌŗģÉ«£¬¼ÓČėĀČĖ®ŗó±äŗģÉ« | øĆČÜŅŗÖŠŗ¬ÓŠFe3+ |
| D | ĻņijČÜŅŗÖŠ¼ÓČėCCl4£¬Õńµ“ŗó¾²ÖĆ | ŅŗĢå·Ö²ć£¬ĻĀ²ć³Ź×ĻŗģÉ« | øĆČÜŅŗÖŠŗ¬ÓŠI- |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬1.56g Na2O2ŗ¬ÓŠµÄŅõĄė×ÓŹżĪŖ0.02NA | |
| B£® | ¹żŃõ»ÆÄĘÓė¶žŃõ»ÆĢ¼·“Ó¦²śÉśŃõĘų0.2mol£¬Ōņ×ŖŅĘ0.8NAµē×Ó | |
| C£® | 0.1molĢśÓėøßĪĀĖ®ÕōĘū·“Ó¦£¬×ŖŅĘ0.3NAµē×Ó | |
| D£® | ±ź×¼×“æöĻĀ£¬22.4L CCl4ŗ¬ÓŠµÄ·Ö×ÓŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 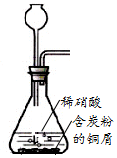 ÓĆ×°ÖĆÖĘČ”NO | |
| B£® |  ÓĆ×°ÖĆŹÕ¼ÆNO | |
| C£® | 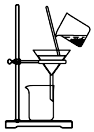 ÓĆ×°ÖĆ·ÖĄėĢæ·ŪŗĶĻõĖįĶČÜŅŗ | |
| D£® | 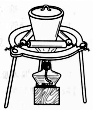 ÓĆ×°ÖĆÕōøÉĻõĖįĶČÜŅŗÖĘCu£ØNO3£©2•3H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com