
为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:下列说法不正确的是( )
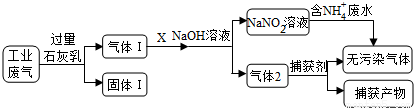
A.固体1中主要含有Ca(OH)2、CaCO3、CaSO3
B.捕获剂所捕获的气体主要是CO
C.X可以是空气,且需过量
D.处理含NH4+废水时,发生反应的离子方程式为:NH4++NO2-==N2↑+2H2O
 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源:2016-2017学年江苏省高二上期中选修化学卷(解析版) 题型:选择题
下列各项叙述中,正确的是
A.分子晶体中不一定存在分子间作用力
B.价电子排布为4s24p1的元素位于第四周期第ⅠA族,是S区元素
C.已知金属钛的晶胞是面心立方结构(如图),则钛晶体1个晶胞中钛原子数为4个

D.水是一种非常稳定的化合物,这是由于氢键所导致
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上期中化学试卷(解析版) 题型:选择题
下列事实可以证明亚硝酸是弱酸的是( )
① 0. 1 mol/L HNO2溶液的pH=2;
1 mol/L HNO2溶液的pH=2;
② HNO2溶液不与Na2SO4溶液反应;
③ HNO2溶液的导电性比盐酸弱;
④ 25℃时NaNO2溶液的pH大于7;
⑤ 将pH=2的HNO2溶液稀释至原体积的100倍,溶液的pH=3.7
A.①③④ B.①④⑤ C.②③④ D.③④⑤
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上期中化学试卷(解析版) 题型:选择题
下列各情况,在其中Fe片腐蚀由快到慢的顺序是( )
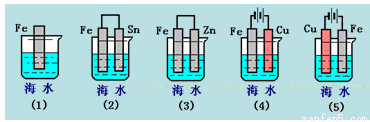
A.(5)(2)(1)(3)(4) B.(2)(5)(3)(4)(1)
C.(5)(3)(4)(1)(2) D.(1)(5)(3)(4)(2)
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上期中化学试卷(解析版) 题型:填空题
工业生产中产生的废气、废液、废渣直接排放会造成污染,很多都经过吸收转化为化工产品。
I.利用电化学原理吸收工业生产中产生的SO2、NO,同时获得Na2S2O4和NH4NO3产品的工艺流程图如图(Ce为铈元素)。
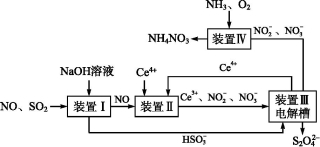
请回答下列问题:
(1)装置Ⅱ中NO在酸性条件下生成NO2-的离子方程式: 。
(2)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示:
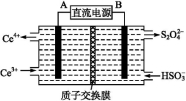
右侧反应室中发生的主要电极反应式为 。
(3)已知进入装置Ⅳ的溶液中NO2-的浓度为0.4 mol·L-1,要使1 m3该溶液中的NO2-完全转化为 NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2的体积为 L。
II.以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:

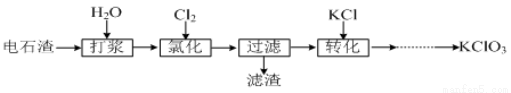
(4)氯化过程控制电石渣过量,在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2 分解为CaCl2和O2。提高Cl2转化为Ca(ClO3)2的转化率的可行措施有 (填序号)。
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(5)氯化过程中Cl2 转化为Ca(ClO3)2的总反应方程式为
6Ca(OH)2+6Cl2===C a(ClO3)2+5CaCl2+6H2O
a(ClO3)2+5CaCl2+6H2O
氯化完成后过滤。滤渣的主要成分为 (填化学式)。
(6)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3 ,若溶液中KClO3的含量为100g?L?1,从该溶液中尽可能多地析出KClO3固体的方法是 。
,若溶液中KClO3的含量为100g?L?1,从该溶液中尽可能多地析出KClO3固体的方法是 。

(7)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) △H=-271kJ/mol
5CaO(s)+H3PO4(l)+HF(g)=Ca5(PO4)3F(s)+5H2O(l) △H=-937kJ/mol
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上期中化学试卷(解析版) 题型:选择题
金属(M)–空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH) n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是( )

A.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B.比较Mg、Al、Zn三种金属–空气电池,Al–空气电池的理论比能量最高
C.在M–空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
D.M–空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne–=4M(OH)n
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上期中化学试卷(解析版) 题型:选择题
X、Y、Z、W是原子序数依次增大的四种短周期元素。其中只有一种是金属元素,X、W同主族且能形成一种离子化合物WX;Y的气态氢化物与其最高价氧化物的水化物可反应生成一种盐;Z原子的最外层电子数与其电子总数之比为3∶4。下列说法中正确的是( )
A. 原子半径:W>Z>Y>X B. 氢化物稳定性:Y>Z
C. WY3中只有离子键没有共价键 D. YX3可用于检验Cl2泄漏
查看答案和解析>>
科目:高中化学 来源:2017届湖南省高三上月考二化学试卷(解析版) 题型:选择题
某溶液中Cl-、Br-、I-个数比为1∶2∶5,欲使这些离子个数比为5∶2∶1,那么要通入Cl2分子个数与原溶液中I-个数比应为( )
A.1∶2 B.2∶1 C.2∶5 D.5∶2
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上学期月考二化学试卷(解析版) 题型:选择题
下列有关原电池的说法中不正确的是
A.由 Al、Cu、稀 H2SO4 组成原电池,放电时 SO42-向 Al 电极移动
B.由 Mg、Al、NaOH 溶液组成原电池,其负极反应式为:Al-3e-+4OH-= AlO2-+2H2O
C.由 Al、Cu、浓硝酸组成原电池作电源,用石墨电极来电解硝酸银溶液,当析出 1 mol Ag时,消耗铜电极32 g
D.由 Fe、Cu、FeCl3 溶液组成原电池,其负极反应式为:Cu-2e-=Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com