
 | 沸点/℃ | 溶解性 |
| SeO2 | 684 | 易溶于水和乙醇 |
| TeO2 | 1260 | 微溶于水,不溶于乙醇 |
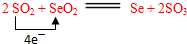 .
. 分析 硒废料中含硒约97%,其余为碲和微量的氯,灼烧过程中,硒、碲分别转化成SeO2、TeO2,SeO2易溶于水和乙醇,TeO2微溶于水,不溶于乙醇,加入试剂A为乙醇,操作Ⅰ为过滤,得到滤渣为TeO2,滤液为SeO2的乙醇溶液,通过蒸馏方法分离得到SeO2和试剂A,
(1)同周期非金属的非金属性强弱判断依据是单质的氧化性、最高价氧化物对应水化物形成酸的酸性、氢化物稳定性、氢化物还原性等,据此分析选项;
(2)周期表中硒和硫位于同主族且相邻,硫为16号元素,则硒为硫的原子序数+第四周期元素种数,原子核外电子层数为周期序数,最外层电子数为主族序数;
(3)增加反应速率的措施是升温、中等压强、增大浓度、加入催化剂、增大接触面积等;
(4)参与反应过程最后又生成的物质可以循环使用,分析可知操作Ⅱ为蒸馏Ⅱ乙醇和二氧化硒;
(5)SeO2和SO2反应发生的是氧化还原反应,二氧化硫被氧化为三氧化硫,二氧化硒被还原为硒单质;
解答 解:硒废料中含硒约97%,其余为碲和微量的氯,灼烧过程中,硒、碲分别转化成SeO2、TeO2,SeO2易溶于水和乙醇,TeO2微溶于水,不溶于乙醇,加入试剂A为乙醇,操作Ⅰ为过滤,得到滤渣为TeO2,滤液为SeO2的乙醇溶液,通过蒸馏方法分离得到SeO2,和试剂A,
(1)同周期非金属的非金属性强弱判断依据是单质的氧化性、最高价氧化物对应水化物形成酸的酸性、氢化物稳定性、氢化物还原性等,
A.沸点:Se>Br2 只能说明分子间作用力强,不能说明非金属性强弱,故A错误;
B.氢化物还原性越强,对应非金属性越弱,H2Se>HBr说明硒的非金属性弱,故B正确;
C.最高价氧化物对应水化物形成的酸的酸性越强,对应非金属性越强,H2SeO4<HBr O4 说明硒的非金属性弱,故C正确;
D.还原性:Se>Br2说明 失电子能力强,则溴的得电子能力强,单质氧化性Se<Br2,证明非金属性溴强,故D正确;
故答案为:A;
(2)周期表中硒和硫位于同主族且相邻,硫为16号元素,则硒为硫的原子序数+第四周期元素种数=16+18=34,硒和硫的原子序数相差18,原子核外电子层数为四层=周期序数,最外层电子数为6=主族序数,则硒元素位于 第四周期ⅥA族,
故答案为:18;第四周期ⅥA族;
(3)增加反应速率的措施是升温、中等压强、增大浓度、加入催化剂、增大接触面积等,在硒废料灼烧过程中,为了提高反应速率,宜采用的措施有粉碎废料、搅拌等,
故答案为:粉碎废料、搅拌;
(4)参与反应过程最后又生成的物质可以循环使用,上述流程中分析可知,可循环利用的物质是乙醇,操作Ⅱ是分离乙醇和二氧化硒的操作为蒸馏,故答案为:乙醇(CH3CH2OH);蒸馏;
(5)SeO2和SO2反应发生的是氧化还原反应,二氧化硫被氧化为三氧化硫,二氧化硒被还原为硒单质,硫元素化合价+4价变化为+6价,吸元素化合价+4价变化为0价,则SeO2和SO2反应和注明电子转移数目和方向的化学方程式为: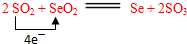
故答案为: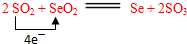 ;
;
点评 本题考查了物质分离提纯方法、实验基本操作、影响化学反应速率的因素、氧化还原反应电子转移等知识点,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ①>②>③>④>⑤ | B. | ②>①>③>④>⑤ | C. | ②>③>④>①>⑤ | D. | ⑤>④>③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | - |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3Cu+8HNO3═3Cu(NO3)2+2NO↑十4H2O | B. | C+4HNO3═CO2↑+4NO2↑十2H2O | ||
| C. | 4HNO3$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑十O2↑十2H2O | D. | NaOH+HNO3═Na NO3十H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某试样焰色反应呈黄色,则试样中一定有钠盐 | |
| B. | 广泛pH试纸测得次氯酸溶液的pH为5 | |
| C. | 温度计不能当作玻璃棒使用 | |
| D. | 粗盐的提纯试验中,滤液在坩埚中加热蒸发结晶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com