
| A. | 50mL 0.15mol•L-1的BaCl2的溶液 | B. | 50mL 0.3mol•L-1的NaCl溶液 | ||
| C. | 25mL 0.3mol•L-1的FeCl3溶液 | D. | 75mL 0.1mol•L-1的KCl溶液 |
分析 电解质溶液中Cl-离子浓度=电解质浓度×化学式中Cl-离子数目,再根据n=cV计算判断.
解答 解:25mL 0.1mol•L-1的AlCl3溶液中的Cl-的物质的量为0.25L×0.1mol•L-1×3=0.075mol,
A.50mL 0.15mol•L-1的BaCl2的溶液中Cl-的物质的量为0.05L×0.15mol•L-1×2=0.015mol,故A不符合;
B.50mL 0.3mol•L-1的NaCl溶液中Cl-的物质的量为0.05L×0.3mol•L-1×1=0.015mol,故B不符合;
C.25mL 0.3mol•L-1的FeCl3溶液中Cl-的物质的量为0.025L×0.3mol•L-1×3=0.0225mol,故C不符合;
D.75mL 0.1mol•L-1的KCl溶液中Cl-的物质的量为0.075L×1mol/L×1=0.075mol,故D符合;
故选D.
点评 本题考查物质的量浓度有关计算,关键是理解电解质离子浓度与电解质浓度关系,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 乙酸是食醋的主要成分,它具有以下化学性质:
乙酸是食醋的主要成分,它具有以下化学性质:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥ | B. | ①②④⑤⑧ | C. | ①②③④⑨ | D. | ②④⑦⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32g O2 | B. | 0.2mol N2 | ||
| C. | 3.01×1023个CO2分子 | D. | 标准状况下11.2L H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
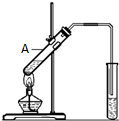
 某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.
某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
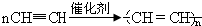 .
.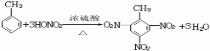 ;该物质的一氯代物有4种.
;该物质的一氯代物有4种.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
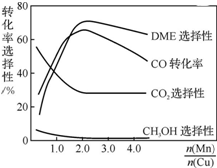 采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(DME).观察上右图回答问题:催化剂中$\frac{n(Mn)}{n(Cu)}$约为2.0时最有利于二甲醚的合成.
采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(DME).观察上右图回答问题:催化剂中$\frac{n(Mn)}{n(Cu)}$约为2.0时最有利于二甲醚的合成.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (I)由短周期元素构成的A~E五种物质中都含有同一种元素,B为单质.
(I)由短周期元素构成的A~E五种物质中都含有同一种元素,B为单质.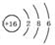 ,A既能与强酸又能与强碱反应,且都能产生气体,请画出A的电子式为
,A既能与强酸又能与强碱反应,且都能产生气体,请画出A的电子式为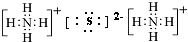 或
或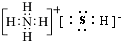 .
.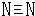
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com