
| A. | 硅酸钠溶液中通入CO2气体:SiO32-+H2O+CO2═H2SiO3↓+CO32- | |
| B. | 硫酸铝与氨水反应:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| C. | 氯气与氢氧化钾溶液反应:Cl2+OH-═Cl-+ClO-+H2O | |
| D. | 小苏打溶液与稀盐酸反应:CO32-+2H+═H2O+CO2↑ |
分析 A.硅酸钠溶液中通入CO2气体,反应生成硅酸沉淀和碳酸钠;
B.二者反应生成硫酸铵和氢氧化铝沉淀;
C.氯气与氢氧化钾溶液反应,实质氯气与水反应生成氯化氢和次氯酸;
D.小苏打为碳酸氢钠,碳酸氢根离子为弱酸的酸式根离子,不能拆.
解答 解:A.硅酸钠溶液中通入CO2气体,离子方程式:SiO32-+H2O+CO2═H2SiO3↓+CO32-,故A正确;
B.硫酸铝与氨水反应,离子方程式:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故B正确;
C.氯气与氢氧化钾溶液反应,实质氯气与水反应生成氯化氢和次氯酸,离子方程式:Cl2+OH-═Cl-+ClO-+H2O,故C正确;
D.小苏打溶液与稀盐酸反应,离子方程式:HCO3-+H+═H2O+CO2↑,故D错误;
故选:D.
点评 本题考查离子反应方程式的书写,明确发生的化学反应及离子反应方程式的书写方法即可解答,题目难度不大.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:解答题
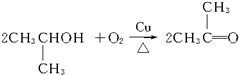 +2H2O)(只写一个)
+2H2O)(只写一个)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2、O3 | B. | Na2O、Na2O2 | ||
| C. | ${\;}_{19}^{40}$K、${\;}_{20}^{40}$Ca | D. | 1H、2H、3H |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
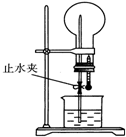 如图装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,然后打开止水夹.下列与实验事实不相符的是( )
如图装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,然后打开止水夹.下列与实验事实不相符的是( )| A. | Cl2(饱和食盐水) 无色喷泉 | B. | NH3(H2O含石蕊) 蓝色喷泉 | ||
| C. | HCl(H2O含石蕊) 红色喷泉 | D. | SO2(NaOH溶液) 无色喷泉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
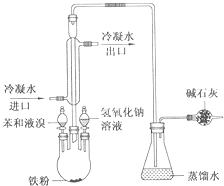 图是实验室制取溴苯的装置图
图是实验室制取溴苯的装置图 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
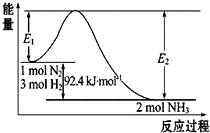 合成氨工业的核心反应是:N2(g)+3H2(g)?2NH3(g)△H=“Q“kJ•mol-1,能量变化如图所示,回答下列问题:
合成氨工业的核心反应是:N2(g)+3H2(g)?2NH3(g)△H=“Q“kJ•mol-1,能量变化如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4H的电子式为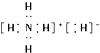 | |
| B. | 1molNH5中含有5NA个N-H键(NA表示阿伏伽德罗常数的数值) | |
| C. | NH4H中的H-半径比锂离子半径大 | |
| D. | NH4H晶体既有共价键又有离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com