
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
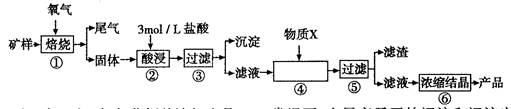
| 金属离子 | 开始形成氢氧化物沉淀的pH | 完全形成氢氧化物沉淀的pH |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
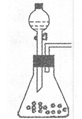
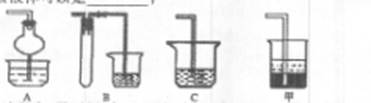
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
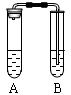
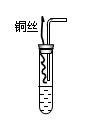
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
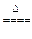 2MgO+Si,同时有副反应发生:2Mg+Si
2MgO+Si,同时有副反应发生:2Mg+Si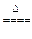 Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4,SiH4在常温下是一种不稳定、易分解的气体(燃烧热约为1430
Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4,SiH4在常温下是一种不稳定、易分解的气体(燃烧热约为1430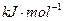 )。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
)。如图是进行Mg与SiO2反应的实验装置,试回答下列问题: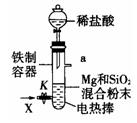
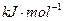 )
)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.取Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒回试剂瓶中。 |
| B.将剩余的金属钠放回原盛放金属钠的试剂瓶中。 |
| C.用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部蒸干才停止加热。 |
| D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
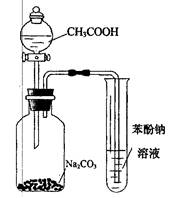
| A.分别加热蒸干灼烧NaAlO2溶液和AlCl3溶液,最终都能得到Al2O3 |
| B.在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,验证Na2CO3溶液中存在水解平衡 |
| C.检验Fe2O3中是杏含有FeO,用盐酸溶解样品后,滴加高锰酸钾溶液,观察溶液紫色是否褪色或变浅 |
| D.利用图示装置并根据有关实验现象能推知酸性: CH3COOH>H2CO3>C6H2OH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B.蒸馏时,温度计水银球应浸没在液体中 |
| C.蒸馏中,冷却水应从冷凝管的下口通入,上口流出。 |
| D.用湿润的红色石蕊试纸检验氨气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稀释浓硫酸时,将蒸馏水沿玻璃棒缓慢注入浓硫酸中 |
| B.用稀硫酸和锌粒反应制氢气时加入少许硫酸铜以加快反应速率 |
| C.用玻璃棒搅拌漏斗中的液体以加快过滤的速度 |
| D.加入盐酸以除去硫酸钠中的少量碳酸钠杂质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com