
准确称取6g铝土矿样品(含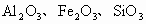 )放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示:
)放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示:
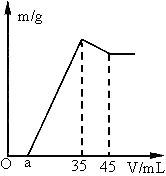
请填空回答:
(1)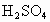 溶液的物质的量浓度为___________________;
溶液的物质的量浓度为___________________;
(2)若a=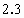 ,用于沉淀
,用于沉淀 消耗NaOH的体积是__________mL,铝土矿中各组成成分的质量分数:
消耗NaOH的体积是__________mL,铝土矿中各组成成分的质量分数: 为__________,
为__________, 为__________,
为__________,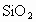 为__________;
为__________;
(3)a值的范围应是__________,在这个范围内,a值越大,__________的质量分数越小.
|
(1)1.75mol/L(2)2.7 ,85%,12%,3%(3)1.625<a<5;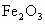 |
|
(1) 由图知,NaOH溶液加至35mL时 、 、 全部沉淀,此时溶液中只存在 全部沉淀,此时溶液中只存在 ,故 ,故
则 
(2) 由
则由图知,溶解  ,消耗的NaOH溶液10mL,则生成这些 ,消耗的NaOH溶液10mL,则生成这些 应消耗同浓度的NaOH溶液30mL,则用于沉淀 应消耗同浓度的NaOH溶液30mL,则用于沉淀 消耗的NaOH溶液的体积为35ML-30mL- 消耗的NaOH溶液的体积为35ML-30mL- mL= mL= mL;所以 mL;所以
所以铝土矿中 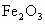 的质量分数为: 的质量分数为:
(3) 由图知,当 、 、 完全沉淀时,共消耗NaOH溶液35mL,而沉淀 完全沉淀时,共消耗NaOH溶液35mL,而沉淀 消耗NaOH溶液30mL,故沉淀 消耗NaOH溶液30mL,故沉淀 和中和过量 和中和过量 共消耗NaOH溶液5mL,所以a<5;因6g铝土矿含 共消耗NaOH溶液5mL,所以a<5;因6g铝土矿含 g,则含 g,则含 的质量小于 的质量小于 g,则生成的 g,则生成的 消耗NaOH溶液的体积 消耗NaOH溶液的体积
因此,在这个范围内, 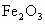 的质量分数越大,a值越小;反之,a值越大, 的质量分数越大,a值越小;反之,a值越大,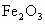 的质量分数越小. 的质量分数越小. |


科目:高中化学 来源: 题型:
铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:

(1)沉淀 A、B的成分分别是 、 ;
(2)步骤②中的试剂a是 ;
(3)试写出步骤③中发生反应的离子方式 ;
(4)准确称取6g铝土矿样品,加入100mL盐酸溶液,充分反应后向滤液中加入10 mol·L-1试剂a的溶液,产生沉淀的质量与加入试剂a的体积关系如下图所示,则所用盐酸溶液的物质的量浓度为 ,样品中Al2O3的百分含量为 。

查看答案和解析>>
科目:高中化学 来源: 题型:
(16分)铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:
(1)沉淀A、B的成分分别是 、 ;
(2)步骤②中的试剂a是 ;
(3)试写出步骤③中发生反应的离子方式 ;
(4)在实验室模拟上述实验过程中,需要用到一定浓度的盐酸溶液。在配制250mi。该盐酸溶液时,某同学转移溶液的操作如图所示,图中的主要错误是:
① ;
② 。
(4)准确称取6g铝土矿样品,加入100mL盐酸溶液,充分反应后向滤液中加入10 mol·L-1试剂a的溶液,产生沉淀的质量与加入试剂a的体积关系如图所示,则所用盐酸溶液的物质的量浓度为 ,样品中Al2O3的百分含量为 。
查看答案和解析>>
科目:高中化学 来源:2010年山东省诸城一中高三上学期第一次月考(化学) 题型:填空题
(16分)铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:
(1)沉淀A、B的成分分别是 、 ;
(2)步骤②中的试剂a是 ;
(3)试写出步骤③中发生反应的离子方式 ;
(4)在实验室模拟上述实验过程中,需要用到一定浓度的盐酸溶液。在配制250mi。该盐酸溶液时,某同学转移溶液的操作如图所示,图中的主要错误是:
① ;
② 。
(4)准确称取6g铝土矿样品,加入100mL盐酸溶液,充分反应后向滤液中加入10 mol·L-1试剂a的溶液,产生沉淀的质量与加入试剂a的体积关系如图所示,则所用盐酸溶液的物质的量浓度为 ,样品中Al2O3的百分含量为 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年广东省梅州市高三上学期期末考试(理综)化学部分 题型:填空题
铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:

(1)沉淀 A、B的成分分别是 、 ;
(2)步骤②中的试剂a是 ;
(3)试写出步骤③中发生反应的离子方式 ;
(4)准确称取6g铝土矿样品,加入100mL盐酸溶液,充分反应后向滤液中加入10 mol·L-1试剂a的溶液,产生沉淀的质量与加入试剂a的体积关系如下图所示,则所用盐酸溶液的物质的量浓度为 ,样品中Al2O3的百分含量为 。

查看答案和解析>>
科目:高中化学 来源:2010年山东省高三上学期第一次月考(化学) 题型:填空题
(16分)铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:

(1)沉淀A、B的成分分别是 、 ;
(2)步骤②中的试剂a是 ;
(3)试写出步骤③中发生反应的离子方式 ;
(4)在实验室模拟上述实验过程中,需要用到一定浓度的盐酸溶液。在配制250mi。该盐酸溶液时,某同学转移溶液的操作如图所示,图中的主要错误是:

① ;
② 。
(4)准确称取6g铝土矿样品,加入100mL盐酸溶液,充分反应后向滤液中加入10 mol·L-1试剂a的溶液,产生沉淀的质量与加入试剂a的体积关系如图所示,则所用盐酸溶液的物质的量浓度为 ,样品中Al2O3的百分含量为 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com