
| A. | Cu | B. | C | C. | Fe | D. | Mg |
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:选择题
| A. |
| |||||||||
| B. |
| |||||||||
| C. | 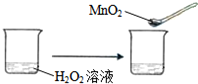 | |||||||||
| D. | 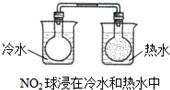 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| B. | 淀粉和蛋白质水解的最终产物都能发生银镜反应 | |
| C. | 油脂都是高级脂肪酸甘油酯,在碱性条件下能发生皂化反应 | |
| D. | “乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、Ca2+、HCO3- | B. | NO3-、Cl-、Na+、Ag+ | ||
| C. | Cu2+、Fe2+、SO42-、Cl- | D. | Mg2+、Na+、Cl-、CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
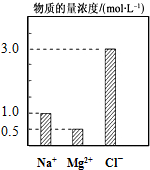 在200mL由NaCl、MgCl2、KCl组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
在200mL由NaCl、MgCl2、KCl组成的混合液中,部分离子浓度大小如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
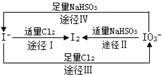
| A. | 由图可知离子还原性的强弱顺序为HSO3->I->Cl- | |
| B. | 足量Cl2能使湿润的淀粉-KI试纸先变蓝后变白 | |
| C. | 途径Ⅱ、Ⅳ反应后溶液的pH均减小 | |
| D. | 途径Ⅲ中若氧化1 mol I-,需消耗67.2L氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | C=O | O=O | C-H | O-H |
| 键能/kJ•mol-1 | 798 | x | 413 | 463 |
| A. | H2O(g)═H2O(l)△S<0,△H=(a-b)kJ/mol | |
| B. | 当有4NA个C-H键断裂时,该反应放出热量一定为a kJ | |
| C. | x=$\frac{1796-b}{2}$ | |
| D. | 利用反应①设计的原电池电解精炼铜时,当负极输出0.2NA个电子时,电解槽的阳极一定减轻6.4g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com