
| A. | 明矾净水:Al3++3H2O?Al(OH)3↓+3H+ | |
| B. | 氯化铵溶于水:NH4++H2O?NH3•H2O+H+ | |
| C. | 亚硫酸溶液中:H2SO3?2H++SO32- | |
| D. | 在小苏打溶液中滴加氢氧化钠:HCO3-+OH-═CO2↑+H2O |
分析 A.铝离子水解生成氢氧化铝胶体,不是氢氧化铝沉淀;
B.铵根离子部分水解生成一水合氨和氢离子;
C.亚硫酸为二元弱酸,其电离分别进行,电离方程式只写出第一步的电离即可;
D.小苏打为碳酸氢钠,碳酸氢钠与氢氧化钠反应生成碳酸钠和水.
解答 解:A.铝离子水解生成氢氧化铝胶体,正确的离子反应方程式为:Al3++3H2O?Al(OH)3+3H+,故A错误;
B.氯化铵溶于水,铵根离子水解,溶液显示酸性,水解的离子方程式为:NH4++H2O?NH3•H2O+H+,故B正确;
C.亚硫酸溶液中,亚硫酸部分电离出氢离子和亚硫酸氢根离子,主要以第一步为主,其正确电离方程式为:H2SO3?H++HSO3-,故C错误;
D.小苏打溶液中滴加氢氧化钠,反应生成碳酸钠和水,正确的离子方程式为:HCO3-+OH-=CO32-+H2O,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握盐的水解原理、弱电解质的电离特点,明确离子方程式正误判断常用方法.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
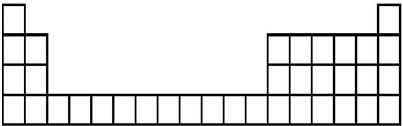
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮的氧化物可形成光化学烟雾和酸雨,能净化空气 | |
| B. | 生水煮沸后会产生水垢,水垢的主要成分中含有Ca(HCO3)2 | |
| C. | Na2CO3和NaHCO3可用澄清石灰水来鉴别 | |
| D. | 等物质的量的Na2CO3、NaHCO3与足量盐酸反应,消耗HCl的物质的量之比为2:1,而放出气体的物质的量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③④ | C. | ②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
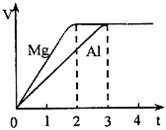 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )| A. | 反应消耗镁、铝的物质的量之比是3:2 | |
| B. | 反应消耗镁、铝的质量之比是3:2 | |
| C. | 与镁和铝反应的硫酸的物质的量之比是3:2 | |
| D. | 与镁和铝反应的硫酸的质量之比是3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com