
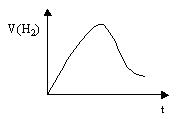
 ½«ZnĶ¶ČėŅ»¶ØÅضČŅ»¶ØĢå»żµÄŃĪĖįÖŠ£¬H2µÄÉś³ÉĖŁĀŹÓėŹ±¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŹŌ½āŹĶĶ¼ÖŠĒśĻß±ä»ÆµÄŌŅņ£Øׯ×ų±źĪŖH2µÄÉś³ÉĖŁĀŹ£¬ŗį×ų±źĪŖŹ±¼ä£©”£
½«ZnĶ¶ČėŅ»¶ØÅضČŅ»¶ØĢå»żµÄŃĪĖįÖŠ£¬H2µÄÉś³ÉĖŁĀŹÓėŹ±¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŹŌ½āŹĶĶ¼ÖŠĒśĻß±ä»ÆµÄŌŅņ£Øׯ×ų±źĪŖH2µÄÉś³ÉĖŁĀŹ£¬ŗį×ų±źĪŖŹ±¼ä£©”£
“š£ŗ¢Ł £»
¢Ś ”£
¢Ł·“Ó¦æŖŹ¼Ź±£¬·“Ó¦·ÅČČ£¬·“Ó¦ĖŁĀŹ½Ļæģ£»¢ŚĖę×Å·“Ó¦µÄ½ųŠŠ£¬HClĪļÖŹµÄĮæÅØ¶Č±äŠ”£¬·“Ó¦ĖŁĀŹÓÖ±äĀż.
±¾ĢāÄÜĮ¦²ć“ĪĪŖC”£ZnÓėŃĪĖį·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬øĆ·“Ó¦ÖŠÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲÓŠĮ½øö£ŗŅ»ŹĒ·“Ó¦·Å³öµÄČČĮæŹ¹·“Ó¦ĖŁĀŹŌö“󣻶žŹĒ·“Ó¦Ź¹HClĪļÖŹµÄĮæÅØ¶Č¼õŠ”£¬·“Ó¦ĖŁĀŹ¼õŠ””£ÓÉĶ¼ĻńæÉÖŖ£¬ŌŚæŖŹ¼Ź±ĪĀ¶Č±ä»ÆŹĒÓ°Ļģ·“Ó¦ĖŁĀŹµÄÖ÷ŅŖŅņĖŲ,µ«Ėę×Å·“Ó¦µÄ½ųŠŠ,HClĪļÖŹµÄĮæÅØ¶ČµÄ¼õŠ”ŹĒÓ°Ļģ·“Ó¦ĖŁĀŹµÄÖ÷ŅŖŅņĖŲ”£“š°ø£ŗ¢Ł·“Ó¦æŖŹ¼Ź±£¬·“Ó¦·ÅČČ£¬·“Ó¦ĖŁĀŹ½Ļæģ£»¢ŚĖę×Å·“Ó¦µÄ½ųŠŠ£¬HClĪļÖŹµÄĮæÅØ¶Č±äŠ”£¬·“Ó¦ĖŁĀŹÓÖ±äĀż.
ѧ·ØÖøµ¼£ŗ±¾Ģāæ¼²éĶعżĶ¼Ļń·ÖĪöÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲ”£Ķ¼Ļń·ÖĪöӦעŅāŅŌĻĀ¼ø·½Ćę£ŗ(1)æ“Ęšµć(2)æ“ÖÕµć(3)擱ä»ÆĒ÷ŹĘ£¬·ÖĒå”°½„±ä”±ŗĶ”°Ķ»±ä”±£¬”°“ó±ä”±ŗĶ”°Š”±ä”±µČ”£


 Č«ÄÜĮ·æ¼¾ķĻµĮŠ“š°ø
Č«ÄÜĮ·æ¼¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
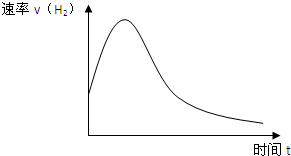 ČēĶ¼±ķŹ¾ZnĶ¶ČėŅ»¶ØÅضČŅ»¶ØĢå»żµÄĻ”H2SO4ČÜŅŗÖŠŗ󣬷“Ó¦Ź±¼äÓėÉś³ÉH2µÄĢå»żµÄĶ¼Ļ󣮣Øׯ×ų±źĪŖH2µÄÉś³ÉĖŁĀŹ£©
ČēĶ¼±ķŹ¾ZnĶ¶ČėŅ»¶ØÅضČŅ»¶ØĢå»żµÄĻ”H2SO4ČÜŅŗÖŠŗ󣬷“Ó¦Ź±¼äÓėÉś³ÉH2µÄĢå»żµÄĶ¼Ļ󣮣Øׯ×ų±źĪŖH2µÄÉś³ÉĖŁĀŹ£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗÉč¼Ę±ŲŠŽ¶ž»ÆѧĖÕ½Ģ°ę ĖÕ½Ģ°ę ĢāŠĶ£ŗ022
ĻĀĶ¼ĖłŹ¾ĪŖ½«ZnĶ¶ČėŅ»¶ØÅضČŅ»¶ØĢå»żµÄH2SO4ČÜŅŗÖŠ£¬½āŹĶĶ¼ĻóµÄ³ÉŅņ(ׯ×ų±źĪŖH2µÄÉś³ÉĖŁĀŹ)£®
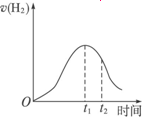
(1)0£t1ĖŁĀŹ±ä»ÆµÄŌŅņŹĒ________£®
(2)t1£t2ĖŁĀŹ±ä»ÆµÄŌŅņŹĒ________£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

(1)0”Ŗt1ĖŁĀŹ±ä»ÆµÄŌŅņŹĒ______________________________”£
(2)t1”Ŗt2ĖŁĀŹ±ä»ÆµÄŌŅņŹĒ______________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĶ¼ĪŖ½«ZnĶ¶ČėŅ»¶ØÅضČĢå»żµÄH2SO4ÖŠ£¬½āŹĶĶ¼ĻńµÄ³ÉŅņ£Øׯ×ų±źĪŖH2µÄÉś³ÉĖŁĀŹ£©
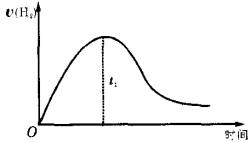
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com